Đề thi giữa HK1 môn Hóa học 11 năm 2020 - Trường THPT Phan Đình Phùng
-
Hocon247
-
30 câu hỏi
-
60 phút
-
11 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Chất nào dưới đây được dùng để điều chế oxi trong phòng thí nghiệm
Các chất để điều chế oxi trong phòng thí nghiệm là hợp chất giàu oxi và dễ phân hủy bởi nhiệt như: KClO3, KMnO4
KClO3 KCl + 3/2 O2↑
2KMnO4 → K2MnO4 + MnO2 + O2↑
Cho hai nguyên tố L và M có cùng cấu hình electron lớp ngoài cùng là ns2. Phát biểu nào sau đây về M và L luôn đúng?
A sai vì nguyên tố có cấu hình 1s2 là khí hiếm (He).
B sai số thứ tự nhóm được xác định dựa theo số electron hóa trị.
C sai vì nguyên tố có 2 electron lớp ngoài cùng có thế là nguyên tố s hoặc nguyên tố d hoặc nguyên tố f …
Dung dịch có pH >7 là
Dung dịch có pH >7 là NaOH → Đáp án B
Hòa tan 2,08 gam hỗn hợp bột gồm FeS, FeS2, S bằng dung dịch H2SO4 đặc nóng dư thu được 2,688 lít SO2 (sp khử duy nhất, đktc) và dung dịch X. Cho dung dịch X tác dụng với dung dịch NaOH dư, lọc lấy toàn bộ kết tủa nung trong không khí đến kl ko đổi thì khối lượng chất rắn thu được là
quy hỗn hợp thành fe, s rồi đặt ẩn là x,y
56x + 32y = 2,08
Bảo toàn e ta có: 3x+4y = 0,24
Tính ra x=0,005, bảo toàn Fe nên mol Fe2O3 bằng 0,0025
m=0,4g
Dãy chất nào dưới đây vừa thể hiện tính khử, vừa thể hiện tính oxi hóa
Cl2, FeO, SO2 vừa thể hiện tính khử, vừa thể hiện tính oxi hóa.
Ta tiến hành sục khí Cl2 vào dung dịch KOH đặc, nóng, dư. Dung dịch thu được có các chất thuộc dãy nào?
Cl2 + KOH → KCl + KClO3 + H2O
Sắp xếp nào dưới đây đúng theo chiều tăng dần tính axit
Dãy sắp xếp theo chiều tăng dần tính axit HClO, HClO2, HClO3, HClO4
Ứng dụng nào sau đây không phải của ozon?
Ozon không dùng để điều chế oxi trong phòng thí nghiệm.
Dãy nào dưới đây tác dụng được với oxi
Fe, Al, C, CH3COOH đều tác dụng được với oxi.
Một hợp chất có thành phần theo khối lượng 35,96% S; 62,92% O và 1,12% H. Hợp chất này có công thức hóa học là
Gọi CT hợp chất là HxSyOz
Ta có x : y : z = %mH/1 : %mS/32 : %mO/16 = 1,12 : 1,12 : 3,935 = 2 : 2 : 7
⇒ CT: H2S2O7
Cho 14,4 gam Cu tác dụng với H2SO4 đặc nóng thu được V lít khí SO2 (đktc). Giá trị của V.
Cu+ 2H2SO4 → CuSO4 + SO2 + 2H2O
nCu = 14,4 : 64 = 0,225 mol
nSO2 = nCu
VSO2 = 5,04 lít
Để phân biệt 4 dung dịch NaCl, HCl, NaNO3, HNO3 ta có thể dùng
Cho quỳ tím vào các dd trên
+ Nhóm 1 các chất làm quỳ hóa đỏ gồm HNO3 và HCl do là các axit
+ Nhóm 2 là các chấ không làm quỳ đổi màu gồm NaCl và NaNO3
Cho nhóm 1 vào dd AgNO3
+ Chất tạo kết tủa trắng với AgNO3 là HCl
PTHH: AgNO3+NaCl → AgCl↓ trắng+NaNO3
+ Chất không có hiện tượng là NaNO3
Cho nhóm 2 cũng vào dd AgNO3
+ Chất tạo kết tủa trắng với AgNO3 là NaCl
PTHH: NaCl + AgNO3 → AgCl↓+NaNO3
+Chất còn lại không pứ là NaNO3
Cho 2,81 gam hỗn hợp A gồm 3 oxit Fe2O3, MgO, ZnO tan vừa đủ trong 300 ml dung dịch H2SO4 0,1M thì khối lượng hỗn hợp các muối sunfat khan tạo ra là
nH2SO4 = 0,3. 0,1 = 0,03 (mol)
Vì phản ứng vừa đủ nên: nO (trong oxit) = nH2SO4 = 0,03 (mol)
→ mO(trong oxit) = 0,03. 16 = 0,48 (g)
→ mH kim loại = 2,81 – 0,48 = 2,33 (g)
Bảo toàn khối lượng: mmuối = mH kim loại + mSO42- = 2,33 + 0,03.96 = 5,21 (g)
Trong phản ứng : Cl2 + SO2 + 2H2O → 2HCl + H2SO4. Clo đóng vai trò :
Trong phản ứng Cl2 + SO2 + 2H2O → 2HCl + H2SO4. Clo đóng vai trò là chất oxi hóa
Hỗn hợp nào sau đây có thể tồn tại trong cùng một dung dịch?
NaNO3 và HCl cùng tồn tại trong 1 dung dịch.
X, Y là hai nguyên tố halogen thuộc hai chu kì liên tiếp trong hệ thống tuần hoàn. Hỗn hợp A có chứa 2 muối của X, Y với natri. Để kết tủa hoàn toàn 2,2 gam hỗn hợp A, phải dùng 150 ml dung dịch AgNO3 0,2M. Tính khối lượng kết tủa thu được?
nAgNO3 = 0,2.0,15 = 0,03
Các phương trình phản ứng:
NaX + AgNO3 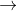 NaNO3 + AgX¯
NaNO3 + AgX¯
NaY + AgNO3 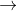 NaNO3 + AgY¯
NaNO3 + AgY¯
Áp dụng định luật bảo toàn khối lượng ta có:
mA + mAgNO3 = mNaNO3 + mkết tủa
2,2 + 0,03.170 = 0,03.85 + mkết tủa
mkết tủa = 4,75 (g)
Cho cân bằng hóa học: 2SO2 (k) + O2 (k) ⇔ 2SO3 (k)
Khi tăng thêm 250C thì tốc độ phản ứng tăng lên 2 lần. Nếu tăng nhiệt độ từ 200C đến 1700C thì tốc độ phản ứng tăng?
Tốc độ phản ứng tăng 64 lần.
Khi tăng nhiệt độ thêm 10oC, tốc độ phản ứng tăng lên 3 lần. Để tốc độ phản ứng ở nhiệt độ 30oC tăng lên 81 lần thì thực hiện phản ứng đó ở nhiệt độ?
Khi nhiệt độ tăng thêm 100C tốc độ phản ứng tăng lên 3 lần.
⇒ Khi nhiệt độ tăng thêm 10.x0C tốc độ phản ứng tăng lên 3x lần.
⇒ 3x = 81 ⇒ x = 4 ⇒ phải tăng thêm 400C.
⇒ Nghĩa là thực hiện phản ứng ở 30 + 40 = 700C.
Cho 14,5 hỗn hợp Mg , Zn và Fe tác dụng hết vs dd H2SO4(l) thấy thoát ra 6,72(l) H2 (dktc). Cô cạn dung dịch sau phản ứng dược khối lượng muối khan là bao nhiêu?
nH2 =
Mg + H2SO4 → MgSO4 + H2
Zn + H2SO4 → ZnSO4 + H2
Fe + H2SO4 → FeSO4 + H2
ta có :
mM = mKL + mSO4
Dùng loại bình nào sau đây để đựng dung dịch HF?
Bình thủy tinh không màu dùng để đựng dung dịch HF
Hấp thụ hoàn toàn 4,48lít SO2 (đktc) vào 200 ml dung dịch KOH 1,5 M. Muối thu được gồm:
nSO2 = 4,48 : 22,4 = 0,05 mol
nKOH = 0,2.1,5 = 0,03 mol
→ Muối thu được gồm: KHSO3 và K2SO3
Đề điều chế V lít oxi (đktc) trong phòng thí nghiệm, người ta nhiệt phân hoàn toàn 3,16 gam KMnO4. Giá trị của V là:
nKMnO = 3,16 : 158 = 0,02 mol
nO2 = 0,01 mol
→ VO2 = 0,01.22,4 = 0,224 lít
Xét cân bằng hóa học sau: 3H2 (k) + N2 (k) ⇔ 2NH3 (k) ![]() H < 0
H < 0
Cân bằng chuyển dịch theo chiều thuận khi.
Các biện pháp làm cân bằng chuyển dịch theo chiều thuận:
+ Giảm nhiệt độ
+ Tăng áp suất
+ Tăng N2 hoặc H2
+ Giảm NH3
Trong số các hiđro halogenua dưới đây, chất nào có tính axit mạnh nhất:
HI có tính axit mạnh nhất
Liên kết cộng hóa trị được tạo thành bằng
Liên kết cộng hóa trị được tạo thành bằng sự góp chung cặp electron của hai nguyên tử.
Đổ dung dịch AgNO3 vào dung dịch chất nào sau đây sẽ thu được kết tủa màu vàng đậm nhất?
AgNO3 + HI → AgI↓ + HNO3
Kết tủa vàng đậm
Xét các phản ứng dưới đây:
(1) H2SO4 + BaCl2 → 2HCl + BaSO4
(2) MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
(3) Fe2O3 + H2SO4 → Fe2(SO4)3 + H2O + SO2
(4) CO2 + Ba(OH)2 → BaCO3 + H2O
(5) KClO3 + 6HCl → Cl2 + KCl + 3H2O
(6) FeS + 2HCl → FeCl2 + H2S
Số phản ứng oxi hóa khử là:
Có tất cả 3 phản ứng oxi hóa khử.
Dãy chất nào dưới đây có thể tác dụng được với HCl?
Fe, KMnO4, NaOH, Fe3O4 có thể tác dụng được với HCl
Cho phản ứng: FeO + H2SO4 → Fe2(SO4)3 + H2O + SO2. Hệ số cân bằng là:
Ta có: 2FeO + 4H2SO4 → Fe2(SO4)3 + 4H2O + 2SO2.
Nguyên tố ở vị trí nào trong bảng tuần hoàn có cấu hình electron hóa trị là 3d64s2?
Cấu hình electron là 1s22s22p63s23p63d64s2
Chu kì 4, 8 e ngoài cùng → VIIIB

