Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Lê Lợi
Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Lê Lợi
-
Hocon247
-
40 câu hỏi
-
90 phút
-
126 lượt thi
-
Dễ
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Đốt cháy hoàn toàn a g triglixerit X cần vừa đủ 4,83 mol khí O2 thì thu được 3,42 mol CO2 và 3,18 mol H2O. Mặt khác a g X phản ứng vừa đủ với NaOH thu được b gam muối. giá trị của b là
X + 4,83 mol O2 → 3,42 mol CO2 + 3,18 mol H2O
Bảo toàn khối lượng có mx = 3,42.44 + 3,18.18 – 4,83,32 = 53,16 gam
Bảo toàn O có 6nx+4,83.2= 3,42.2+3,18![]() nx= 0,06
nx= 0,06
X+ 3NaOH →muối + glixerol
Ta có nNaOH = 0,18 mol và nglixerol = 0,06 mol
Bảo toàn khối lượng có mx + mNaOH = m muối + mglixerol
→53,16 + 0, 18.40 = b + 0,06.92
→ b = 54,84
Cho 115,3 gam hỗn hợp 2 muối MgCO3 và RCO3 vào dung dịch H2SO4 loãng, thu được 4,48 lít khí CO2 đktc, chất rắn X và dung dịch Y chứa 12 gam muối. Nung X đến khối lượng không đổi, thu được chất rắn Z và 11,2 lít khí CO2 đktc. Khối lượng của Z là
115,3 gam RCO3 , MgCO3 thì CO32- + 2H+ →H2O + CO2
Ta có nH2SO4 = nCO2 = nH2O = 0,2 mol
Bảo toàn khối lượng có
muối ban đầu + mH2SO4 = muối + mCO2 + mx + mH2O
→ 115,3 + 0,2.98 = 12 + mX + 0,2.44 +0,2.18 → mx = 110,5 g
X → Z + 0,5 mol CO2
Bảo toàn khối lượng có mz = mx- mCO2 = 110,5 – 0,5.44 = 88,5g
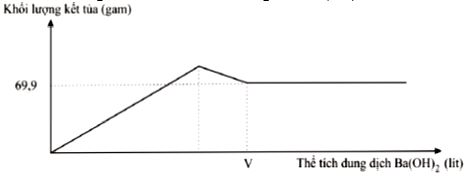
Nhỏ từ từ dung dịch Ba(OH)2 0,2M vào ống nghiệm chứa dung dịch Al2(SO4)3. Đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa theo thể tích dung dịch Ba(OH)2 như sau:
Giá trị của V gần nhất với giá trị nào sau đây?
Tại V thì kết tủa chỉ chứa BaSO4 với nBaSO4 = 0,3 mol
→ nAl2(SO4)3 = 0,1 mol
nBa(OH)2 = 4nAl3+/2 = 0,4 mol
V Ba(OH)2 = 2 lít Chọn B
Thủy phân hoàn toàn tinh bột, thu được monosaccarit X. Hiđro hóa X, thu được chất hữu cơ Y. Hai chất X, Y lần lượt là:
Thủy phân hoàn toàn tinh bột, thu được monosaccarit X. Hiđro hóa X, thu được chất hữu cơ Y. Hai chất X, Y lần lượt là glucozơ, sobitol.
Dung dịch glyxin (axit α-aminoaxetic) phản ứng được với dung dịch nào sau đây?
Dung dịch glyxin (axit α-aminoaxetic) phản ứng được với dung dịch HCl
Tripanmitin là chất béo no, ở trạng thái rắn. Công thức của tripanmitin là
Công thức của tripanmitin là (C15H31COO)3C3H5
Poli(metyl metacrylat) (PMM) được điều chế từ phản ứng trùng hợp chất nào sau đây?
Poli(metyl metacrylat) (PMM) được điều chế từ phản ứng trùng hợp CH2=C(CH3)COOCH3.
Kim loại nào sau đây có số oxi hóa +1 duy nhất trong hợp chất?
K có số oxi hóa +1 duy nhất trong hợp chất
Hợp chất nào sau đây không có tính lưỡng tính?
AlCl3 không có tính lưỡng tính
Manhetit là một loại quặng sắt quan trọng, nhưng hiếm có trong tự nhiên, dùng để luyện gang, thép. Thành phần chính của quặng manhetit là gì?
Thành phần chính của quặng manhetit là Fe3O4
Đốt cháy 2,15 gam hỗn hợp gồm Zn, Al và Mg trong khí oxi dư, thu được 3,43 gam hỗn hợp X. Toàn bộ X phản ứng vừa đủ với V ml dung dịch HCl 0,5M. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là
\(+ \,\,BTN T:\,\,{n_{{H^ + }}} = 2{n_{{O^{2 - }}}} = \frac{{3,43 - 2,15}}{{16}} = 0,16 \Rightarrow {V_{dd\,\,HCl}} = \frac{{0,16}}{{0,5}} = 0,32\,\,li t = \boxed{320\,\,ml}\)
Để trung hòa 25 gam dung dịch của một amin đơn chức X nồng độ 12,4% cần dùng 100 ml dung dịch HCl 1M. Công thức phân tử của X là
\(+ \,\,\left\{ \begin{gathered} {m_{{C_x}{H_y}N}} = 25.12,4\% = 3,1\,\,gam \hfill \\ {n_{{C_x}{H_y}N}} = {n_{HCl}} = 0,1\,\,mol \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} {M_{{C_x}{H_y}N}} = 31 \hfill \\ {C_x}{H_y}N\,\,la{o}\,\,\boxed{C{H_5}N} \hfill \\ \end{gathered} \right.\)
Cho các polime: poli(vinyl clorua), xenlulozơ, policaproamit, polistiren, xenlulozơ triaxetat, nilon-6,6. Số polime tổng hợp?
Số polime tổng hợp: poli(vinyl clorua), policaproamit, polistiren, nilon-6,6.
Phát biểu nào sau đây khi so sánh 3 kim loại Mg, Al, Cr là đúng?
Đáp án B đúng, các đáp án còn lại đều sai ở các điểm sau đây:
- Cr ở nhóm VIB trong bảng tuần hoàn.
- Al phản ứng với HCl theo tỷ lệ 1:3 trong khi Mg và Cr theo tỷ lệ 1:2.
- Tính khử giảm theo thứ tự Mg, Al, Cr.
Dung dịch X có 0,1 mol K+; 0,2 mol Mg2+; 0,1 mol Na+; 0,2 mol Cl- và a mol Y-. Ion Y- và giá trị của a là
Vì có Mg2+ nên dung dịch không có OH- → Loại B và C.
\(\xrightarrow{{BTDT}}0,1 + 0,2.2 + 0,1 = 0,2 + a\xrightarrow{{}}a = 0,4\)
Cho 6 gam một oxit kim loại hóa trị II tác dụng vừa đủ với HCl cho 14,25 gam muối clorua của kim loại đó. Cho biết công thức oxit kim loại?
\(\xrightarrow{{BTNT.M}}{n_M} = \frac{6}{{M + 16}} = \frac{{14,25}}{{M + 71}}\,\,\,\,\,\,\, \to M = 24\,\,\,Mg\)
Vật liệu bằng nhôm khá bền trong không khí là do
Vật liệu bằng nhôm khá bền trong không khí là do có lớp oxit bào vệ.
Phát biểu nào sau đây là đúng?
Trong tự nhiên, các kim loại kiềm tồn tại dưới dạng hợp chất.
Cho 9,2 gam Na vào 300 ml dung dịch HCl 1M cô cạn dung dịch sau phản ứng được số gam chất rắn khan là:
\(m\left\{ \begin{gathered} N{a^ + }:0,4 \hfill \\ C{l^ - }:0,3 \hfill \\ \xrightarrow{{BTDT}}O{H^ - }:0,1 \hfill \\ \end{gathered} \right.\xrightarrow{{BTKL}}m = 21,55\)
Đốt cháy hoàn toàn m gam chất béo X (chứa triglixerit của axit stearic, axit panmitic và các axit béo tự do đó). Sau phản ứng thu được 20,16 lít CO2 (đktc) và 15,66 gam nước. Xà phòng hóa m gam X (H = 90%) thì thu được khối lượng glixerol là
\(\left\{ \begin{gathered} {n_{{C_3}{H_5}{{(OOC\overline R )}_3}}} = 0,015 \hfill \\ {n_{{C_3}{H_5}{{(OH)}_3}}} = 90\% {n_X} = 0,0135\,\,mol \Leftrightarrow \boxed{1,242\,\,gam} \hfill \\ \end{gathered} \right.\)
Hỗn hợp khí X gồm propen, etan, buta-1,3-đien, but-1-in có tỉ khối hơi so với SO2 là 0,75. Đốt cháy hoàn toàn 0,02 mol hỗn hợp X, cho hấp thụ toàn bộ sản phẩm cháy vào bình dung dịch Ca(OH)2 dư thì thu được m gam kết tủa. Giá trị của m là
\(\begin{gathered} + \,\,\left\{ \begin{gathered} X\,\,gom\,\,{C_3}{H_6},\,\,{C_2}{H_6},\,\,{C_4}{H_6}\overset {quy\,\,doi} \leftrightarrows {C_{\overline n }}{H_6} \hfill \\ {\overline M _X} = 12\overline n + 6 = 0,75.64 = 48 \hfill \\ \end{gathered} \right. \Rightarrow \overline n = 3,5. \hfill \\ + \,\,\left\{ \begin{gathered} \underbrace {{C_{3,5}}{H_6}}_{0,02\,\,mol}\xrightarrow{{{O_2},\,\,{t^o}}}\underbrace {C{O_2}}_{0,07\,\,mol}\xrightarrow{{Ca{{(OH)}_2}\,\,du}}\underbrace {CaC{O_3}}_{0,07\,\,mol} \hfill \\ {m_{CaC{O_3}}} = 100.0,07 = \boxed{7\,\,gam} \hfill \\ \end{gathered} \right. \hfill \\ \end{gathered} \)
Cho 40 gam hỗn hợp X gồm Fe3O4 và Cu vào dung dịch HCl, thu được dung dịch Y chứa hai chất tan và còn lại 16,32 gam chất rắn. Cho dung dịch AgNO3 dư vào dung dịch Y, thu được m gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
\(\begin{gathered} + \,BTE:\,\,{n_{F{e_3}{O_4}}} = {n_{Cu\,\,pu}} = x \Rightarrow 232x + 64x = 40 - 16,32 \Rightarrow x = 0,08. \hfill \\ + \,\,\left\{ \begin{gathered} FeC{l_2}:\,\,0,24\,\,mol \hfill \\ CuC{l_2}:\,\,0,08\,\,mol \hfill \\ \end{gathered} \right\}\xrightarrow{{AgN{O_3}\,\,du}}\left\{ \begin{gathered} Ag \downarrow :\,\,0,24\,\,mol \hfill \\ AgCl \downarrow :\,\,0,64\,\,mol \hfill \\ \end{gathered} \right\} \Rightarrow {m_{ket\,tua}} = 117,76 \approx \,\boxed{118} \hfill \\ \end{gathered} \)
Hấp thụ hoàn toàn 8,96 lít CO2 (đktc) và 500 ml dung dịch gồm NaOH 0,5M, KOH 0,6M, thu được dung dịch X. Khối lượng chất tan trong X là
\( + \,\,\left\{ \begin{gathered} \left\{ \begin{gathered} NaOH:\,\,0,25 \hfill \\ KOH:\,\,0,3 \hfill \\ \end{gathered} \right\} + \underbrace {C{O_2}}_{0,4}\overset {quy\,\,doi} \leftrightarrows \left\{ \begin{gathered} NaOH:\,\,0,25 \hfill \\ KOH:\,\,0,3 \hfill \\ \end{gathered} \right\} + \underbrace {{H_2}C{O_3}}_{0,4}\xrightarrow{{}}chat\,\,\tan + \underbrace {HOH}_{0,55} \hfill \\ BTKL:\,\,{m_{chat\,\,\tan }} = {m_{bazo}} + {m_{{H_2}C{O_3}}} - {m_{{H_2}O}} = \boxed{41,7\,\,gam} \hfill \\ \end{gathered} \right.\)
Dung dịch X có màu da cam. Nếu cho thêm vào một lượng KOH, màu đỏ của dung dịch dần dần chuyển sang màu vàng tươi. Nếu thêm vào đó một lượng H2SO4, màu của dung dịch dần dần trở lại màu da cam. Dung dịch X chứa chất có công thức phân tử là
\(\begin{gathered} 2CrO_4^{2 - } + 2{H^ + } \rightleftarrows C{r_2}O_7^{2 - } + {H_2}O \hfill \\ {\text{(vang}})\,\,\,\,\,\,\,\,\,\,\,\,\,{\text{(da cam)}} \hfill \\ \end{gathered} \)
Các dung dịch riêng biệt: Na2CO3, BaCl2, MgCl2, H2SO4, NaOH được đánh số ngẫu nhiên (1), (2), (3), (4), (5). Tiến hành một số thí nghiệm, kết quả được ghi lại trong bảng sau:
Các dung dịch (1), (3), (5) lần lượt là H2SO4, NaOH, MgCl2.
Cho 200 ml dung dịch amino axit X nồng độ 0,4M tác dụng vừa đủ với 80 ml dung dịch NaOH 1M, thu được dung dịch chứa 10 gam muối. Khối lượng mol phân tử của X là
\(\begin{gathered} + \,\,\left\{ \begin{gathered} {n_{ - COOH/X}} = {n_{NaOH}} = 0,08 \hfill \\ {n_X} = 0,08 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} X\,\,la{}\,\,{({H_2}N)_n}RCOOH:0,08\,\,mol \hfill \\ muoi\,\,la{}\,\,{({H_2}N)_n}RCOONa:0,08\,\,mol \hfill \\ \end{gathered} \right. \hfill \\ \Rightarrow {M_{muoi}} = \frac{{10}}{{0,08}} = 125 \Rightarrow {M_X} = 125 - 22 = \boxed{103} \hfill \\ \end{gathered} \)
Người ta dùng glucozơ để tráng ruột phích. Trung bình cần dùng 0,75 gam glucozơ cho một ruột phích. Tính khối lượng Ag có trong ruột phích biết hiệu suất phản ứng là 80%.
\(\,{n_{Ag}} = 2{n_{glucozo}} = 2.\frac{{0,75.80\% }}{{180}}\,\,mol \Rightarrow {m_{Ag}} = 2.\frac{{0,75.80\% }}{{180}}.108 = \boxed{0,72\,\,gam}\)
Hỗn hợp X gồm 4 chất hữu cơ đều có cùng công thức phân tử C2H8O3N2. Cho một lượng X phản ứng vừa đủ với V ml dung dịch NaOH 0,5M và đun nóng, thu được dung dịch Y chỉ gồm các chất vô cơ và 6,72 lít (đktc) hỗn hợp Z gồm 3 amin. Cô cạn toàn bộ dung dịch Y thu được 29,28 gam hỗn hợp muối khan. Giá trị của V là
\(\begin{gathered} + \,\,\left\{ \begin{gathered} X\xrightarrow{{NaOH}}a\min + muoi \hfill \\ X\,\,co\,CTPT{C_2}{H_8}{O_3}{N_2} \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} X\,\,la\,\,muoi\,\,amoni \hfill \\ co\,goc\,{\text{ax}}it:\,\,N{O_3};\,\,C{O_3};\,\,HC{O_3} \hfill \\ \end{gathered} \right. \hfill \\ + \,\,4\,\,chat\,\,trong\,\,X\,\,la:\,\,\left\{ \begin{gathered} {C_2}{H_5}N{H_3}N{O_3};\,\,{(C{H_3})_2}N{H_2}N{O_3} \hfill \\ C{H_2}{(N{H_3})_2}C{O_3};\,\,{H_2}NC{H_2}N{H_3}HC{O_3} \hfill \\ \end{gathered} \right. \hfill \\ + \,\,So\,\,do\,phan\,\,ung: \hfill \\ \,\,\,\,\,\,\,\left\{ \begin{gathered} \left\{ \begin{gathered} {C_2}{H_5}N{H_3}N{O_3} \hfill \\ {(C{H_3})_2}N{H_2}N{O_3} \hfill \\ \end{gathered} \right\}:\,\,x\,\,mol \hfill \\ \left\{ \begin{gathered} C{H_2}{(N{H_3})_2}C{O_3} \hfill \\ {H_2}NC{H_2}N{H_3}HC{O_3} \hfill \\ \end{gathered} \right\}:\,\,y\,\,mol \hfill \\ \end{gathered} \right\}\xrightarrow{{NaOH}}\left\{ \begin{gathered} \left\{ \begin{gathered} {C_2}{H_5}N{H_2} \hfill \\ {(C{H_3})_2}NH \hfill \\ \end{gathered} \right\}:\,\,x\,\,mol \hfill \\ C{H_2}{(N{H_2})_2}:\,\,y\,\,mol \hfill \\ \end{gathered} \right\} + \,\,\left\{ \begin{gathered} \underbrace {NaN{O_3}}_{x\,\,mol} \hfill \\ \underbrace {N{a_2}C{O_3}}_{y\,\,mol} \hfill \\ \end{gathered} \right\} \hfill \\ \Rightarrow \left\{ \begin{gathered} x + y = 0,3 \hfill \\ 85x + 106y = 29,28 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} x = 0,12 \hfill \\ y = 0,18 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} {n_{NaOH}} = x + 2y = 0,48 \hfill \\ {V_{dd\,\,NaOH\,\,0,5M}} = 0,96\,\,lit = \boxed{960\,\,ml} \hfill \\ \end{gathered} \right. \hfill \\ \end{gathered} \)
Dung dịch X chứa 0,6 mol NaHCO3 và 0,3 mol Na2CO3. Thêm rất từ từ dung dịch chứa 0,8 mol HCl vào dung dịch X, thu được dung dịch Y và V lít khí CO2 (đktc). Thêm vào dung dịch Y nước vôi trong dư thấy tạo thành m gam kết tủa. Thể tích khí CO2 và khối lượng kết tủa là
\(\begin{gathered} {n_{C{O_2}}} = {n_{{H^ + }}} - {n_{C{O_3}^{2 - }}} = 0,5\,\,mol \Rightarrow \boxed{{V_{C{O_2}}} = 11,2\,\,li{\text{t}}} \hfill \\ {n_{CaC{O_3}}} = {n_{HC{O_3}^ - /Y}} = {n_{C{O_3}^{2 - }}} + {n_{HC{O_3}^ - \,\, }} - {n_{C{O_2}}} = 0,4 \Rightarrow \boxed{{m_{CaC{O_3}}} = 40\,\,gam} \hfill \\ \end{gathered} \)
Nung bột Fe2O3 với a gam bột Al trong khí trơ, thu được 11,78 gam hỗn hợp rắn X. Cho toàn bộ X vào lượng dư dung dịch NaOH, thu được 1,344 lít H2 (đktc). Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của a là
\(\begin{gathered} \,\left\{ \begin{gathered} F{e_2}{O_3}:\,\,x\,\,mol \hfill \\ Al \hfill \\ \end{gathered} \right\}\xrightarrow{{{t^o}}}\underbrace {\left\{ \begin{gathered} Fe:\,\,2x\,\,mol \hfill \\ A{l_2}{O_3}:\,\,x\,\,mol \hfill \\ Al\,\,du:\,\,y \hfill \\ \end{gathered} \right\}}_{{m_X} = 11,78\,\,gam}\xrightarrow{{NaOH}}NaAl{O_2} + \underbrace {{H_2} \uparrow }_{0,06\,\,mol} \hfill \\ + \,\,\left\{ \begin{gathered} {m_X} = 11,78 \hfill \\ BTE:\,\,3{n_{Al\,\,du}} = 2{n_{{H_2}}} \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} 2x.56 + 102x + 27y = 11,78 \hfill \\ 3y = 2.0,06 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} y = 0,04 \hfill \\ x = 0,05 \hfill \\ \end{gathered} \right. \hfill \\ \Rightarrow {n_{Al\,\,ban\,\,dau}} = 2x + y = 0,14 \Rightarrow \boxed{{m_{Al}} = 3,78\,\,gam} \hfill \\ \end{gathered} \)
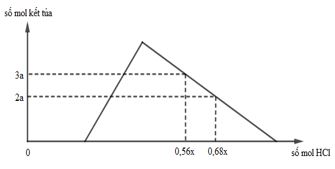
Hỗn hợp X gồm Al, Ca, Al4C3 và CaC2. Cho 40,3 gam X vào nước dư, chỉ thu được dung dịch Y và hỗn hợp khí Z (C2H2, CH4, H2). Đốt cháy hết Z thu được 20,16 lít khí CO2 (đktc) và 20,7 gam H2O. Nhỏ từ từ V lít dung dịch HCl xM vào Y, được biểu diễn theo hình vẽ:
Giá trị của x gần nhất với
\(\begin{gathered} + \,\,{m_{{O^{2 - }}}} = 0,2m\,\,gam \Leftrightarrow x\,\,mol \Rightarrow m = 80x. \hfill \\ + \,\,{m_{A{l_2}{O_3}}} = 102.\frac{x}{3} = 34{\text{x}} \Rightarrow \left\{ \begin{gathered} {n_K} + 2{n_{Ba}} = 0,022.2 \hfill \\ 39{n_K} + 137{n_{Ba}} = 46{\text{x}} \hfill \\ \end{gathered} \right. \Rightarrow {n_{Ba}} = \frac{{46{\text{x}} - 1,716}}{{59}}. \hfill \\ {O^{2 - }} + {H_2}O + {H^ + }\xrightarrow{{}}O{H^ - } + {H_2} \uparrow \hfill \\ \,x\,\,\,\,\,\,\,\,\,\,\,\,\,y\,\,\,\,\,\,\,\,\,\,0,074\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,022 \hfill \\ \Rightarrow BT\,\,O:\,\,{n_{O{H^ - }}} = x + y. \hfill \\ \Rightarrow \left\{ \begin{gathered} BTKL:\,\,16x + 18y + 0,074 = 17(x + y) + 0,022.2 \hfill \\ {m_{ket\,tua}} = 78.\frac{{(x + y)}}{3} + 233.\frac{{46{\text{x}} - 1,716}}{{59}} = 2,958 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} x = 0,045 \hfill \\ y = 0,015 \hfill \\ \end{gathered} \right. \Rightarrow \boxed{m = 3,6\,\,gam} \hfill \\ \end{gathered} \)
Cho các polime: poliacrilonitrin, poli(phenol-fomanđehit), poli(hexametylen–ađipamit), poli(etylen-terephtalat), polibutađien, poli(metyl metacrylat). Số polime dùng làm chất dẻo là
Số polime dùng làm chất dẻo là poli(phenol-fomanđehit), poli(metyl metacrylat).
Cho các phát biểu sau:
(a) Cho dung dịch Na2SO4 vào dung dịch Ba(OH)2, thu được dung dịch chứa NaOH.
(b) Nước tự nhiên thường có cả tính cứng tạm thời và tính cứng vĩnh cửu.
(c) Để điều chế Mg, Al người ta dùng khí H2 hoặc CO để khử oxit kim loại tương ứng ở nhiệt độ cao.
(d) Công thức hóa học của thạch cao nung là CaSO4.2H2O.
(e) Dùng bình cứu hỏa để dập tắt đám cháy có mặt Mg.
Số phát biểu đúng là
Số phát biểu đúng là a, b
Cho các phát biểu sau:
(a) Hợp kim Na - K có nhiệt độ nóng chảy thấp, 70oC.
(b) NaOH là chất rắn, màu trắng, dễ nóng chảy, hút ẩm mạnh, tan nhiều trong nước và tỏa ra một lượng nhiệt lớn.
(c) Al(OH)3, NaHCO3, Al2O3là các chất có tính chất lưỡng tính.
(d) Có thể điều chế kim loại nhôm bằng cách điện phân nóng chảy muối halogenua của nó.
(e) Kim loại xesi dùng làm tế bào quang điện;
Số phát biểu đúng là
Số phát biểu đúng là 3
Cho các phát biểu sau:
(a) Một số este có mùi thơm, không độc, được dùng làm hương liệu trong công nghiệp thực phẩm, mĩ phẩm,...
(b) Gạo nếp chứa nhiều amilopectin hơn gạo tẻ.
(c) Dung dịch các amino axit có thể làm đổi màu quỳ tím sang đỏ hoặc sang xanh hoặc không làm đổi màu.
(d) Khi nấu canh cua thì thấy các mảng “riêu cua” nổi lên là do sự đông tụ của protein do nhiệt độ.
(e) Phản ứng thủy phân chất béo trong môi trường kiềm là phản ứng thuận nghịch.
(g) Một số polime như xenlulozơ, poli(haxametylen điamin), poliacrilonitrin được dùng làm tơ.
Số phát biểu đúng là
Số phát biểu đúng là a, b, c, d, g
Cho 100ml dung dịch HCl 0,1M vào 100ml dung dịch Ba(OH)2 0,06M thu được 200ml dung dịch X. Giá trị pH của dung dịch X là:
\(\left\{ \begin{gathered} {n_{{H^ + }}} = 0,01(mol) \hfill \\ {n_{O{H^ - }}} = 0,012(mol) \hfill \\ \end{gathered} \right.\xrightarrow{{}}\left[ {O{H^ - }} \right] = \frac{{0,012 - 0,01}}{{0,2}} = {10^{ - 2}}\)
\(\xrightarrow{{}}\left[ {{H^ + }} \right] = {10^{ - 12}}\xrightarrow{{}}pH = 12\)
Hòa tan hoàn toàn 1,62 gam Al trong 280 ml dung dịch HNO3 1M, thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Cho 5,75 gam kim loại Na và 500 ml dung dịch HCl, thu được dung dịch Y. Trộn dung dịch X với dung dịch Y tạo thành 1,56 gam kết tủa. Nồng độ mol của dung dịch HCl là
\(+ \,\,BTE:\,\,{n_{NO}} = {n_{Al}} = 0,06\)
\( \Rightarrow \underbrace {Al}_{0,06\,\,mol} + \underbrace {HN{O_3}}_{0,28\,\,mol} \to \underbrace {NO}_{0,06\,\,mol} + \underbrace {\left\{ \begin{gathered} Al{(N{O_3})_3}:\,\,0,06\,\,mol \hfill \\ HN{O_3}:\,\,0,28 - 0,06.4 = 0,04\,\,mol \hfill \\ \end{gathered} \right\}}_{dd\,\,X}\)
\(+ \,\,\underbrace {Na}_{0,25} + HCl \to \underbrace {\left\{ \begin{gathered} NaCl:\,\,x\,\,mol \hfill \\ NaOH:\,\,y\,\,mol \hfill \\ \end{gathered} \right\}}_{dd\,\,Y}\)
\( + \,\,\underbrace {\left\{ \begin{gathered} Al{(N{O_3})_3}:\,\,0,06 \hfill \\ HN{O_3}:\,\,0,04 \hfill \\ \end{gathered} \right\}}_{dd\,\,X} + \underbrace {\left\{ \begin{gathered} NaCl:\,\,x \hfill \\ NaOH:\,\,y \hfill \\ \end{gathered} \right\}}_{dd\,\,Y} \to 0,02\,\,mol\,\,Al{(OH)_3} \downarrow \)
TH1: Al(OH)3 không bị hòa tan
\( \Rightarrow \left\{ \begin{gathered} y = {n_{O{H^ - }}} = {n_{{H^ + }}} + 3{n_{Al{{(OH)}_3}}} = 0,1 \hfill \\ {n_{Na}} = x + y = 0,25 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} y = 0,1 \hfill \\ x = 0,15 \hfill \\ \end{gathered} \right. \Rightarrow [HCl] = \frac{{0,15}}{{0,5}} = \boxed{0,3M}\)
TH2: Al(OH)3 bị hòa tan một phần
\(\Rightarrow \left\{ \begin{gathered} y = {n_{O{H^ - }}} = {n_{{H^ + }}} + 3{n_{A{l^{3 + }}}} + ({n_{A{l^{3 + }}}} - {n_{Al{{(OH)}_3}}}) = 0,26 \hfill \\ {n_{Na}} = x + y = 0,25 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} y = 0,26 \hfill \\ x = - 0,01 \hfill \\ \end{gathered} \right. \Rightarrow Vo\,\,li\)
Hòa tan hoàn toàn 8,6 gam hỗn hợp Al, Mg, Fe, Zn vào 100 gam dung dịch gồm KNO3 1M và H2SO4 2M, thu được dung dịch X chứa 43,25 gam muối trung hòa và hỗn hợp khí Y (trong đó H2 chiếm 4% khối lượng Y). Cho một lượng KOH vào X, thu được dung dịch chỉ chứa một chất tan và kết tủa Z (không có khí thoát ra). Nung Z trong không khí đến khối lượng không đổi được 12,6 gam chất rắn. Nồng độ phần trăm của FeSO4 trong X gần giá trị nào nhất sau đây?
\(X\,\,\left\{ \begin{gathered} MgS{O_4},\,\,FeS{O_4},\,\,F{e_2}{(S{O_4})_3} \hfill \\ A{l_2}{(S{O_4})_3},\,\,ZnS{O_4},\,\,{K_2}S{O_4} \hfill \\ \end{gathered} \right.\)
\(\begin{gathered} + \,\,{n_{KN{O_3}}} = x;\,\,{n_{{H_2}S{O_4}}} = 2x \Rightarrow {m_{muoi/X}} = 8,6 + 39x + 2x.96 = 43,25 \Rightarrow x = 0,15. \hfill \\ + \,\,{n_{{H_2}}} = y \Rightarrow {m_Y} = 50y,\,\,{n_{{H_2}O}} = 0,3 - y. \hfill \\ + \,\,\left\{ \begin{gathered} BTKL:\,\,{m_{kl}} + {m_{(KN{O_3},\,\,{H_2}S{O_4})}} = {m_{muoi}} + {m_Y} + {m_{{H_2}O}} \hfill \\ BTKL:\,\,{m_{kl}} + {m_{dd\,\,(KN{O_3},\,\,{H_2}S{O_4})}} = {m_{dd\,\,X}} + {m_Y} \hfill \\ \end{gathered} \right. \hfill \\ \Rightarrow \left\{ \begin{gathered} 8,6 + 0,15.101 + 0,3.98 = 43,25 + 50y + 18(0,3 - y) \hfill \\ 8,6 + 100 = {m_{dd\,\,X}} + 50y \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} y = 0,140625 \hfill \\ {m_{dd\,\,X}} = 101,56875 \hfill \\ \end{gathered} \right. \hfill \\ + \,\,KOH + X\xrightarrow{{}}dd\,\,{K_2}S{O_4} + \,\,Z \downarrow \Rightarrow \left\{ \begin{gathered} {n_{KOH}} = 2{n_{{K_2}S{O_4}}} - {n_{KN{O_3}}} = 0,45 \hfill \\ {n_{O{H^ - }\,\,trong\,\,Z}} = {n_{KOH}} = 0,45 \hfill \\ \end{gathered} \right. \hfill \\ + \,\,Khi\,\,nung\,\,Z\left\{ \begin{gathered} 0,45\,\,mol\,\,O{H^ - }\xrightarrow{{}}0,225\,\,mol\,\,{O^{2 - }} \hfill \\ {O_2}\xrightarrow{{oxh\,F{e^{2 + }}}}\,\,z\,\,mol\,\,{O^{2 - }} \hfill \\ \end{gathered} \right. \hfill \\ \Rightarrow 0,225.16 + 16z = 12,6 - 8,6 \Rightarrow z = 0,025 \Rightarrow BTE:\,\,{n_{F{e^{2 + }}}} = 2{n_{{O^{2 - }}}} = 0,05 \hfill \\ \Rightarrow C{\% _{FeS{O_4}}} = \frac{{152.0,05}}{{101,56875}}.100\% = 7,48\% \,\, \hfill \\ \end{gathered} \)
Điện phân dung dịch X gồm CuSO4 và KCl (tỉ lệ mol tương ứng là 1 : 5) với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi I = 2A. Sau 1930 giây, thu được dung dịch Y và hỗn hợp khí gồm H2 và Cl2 (có tỉ khối so với H2 là 24). Mặt khác, nếu điện phân X trong thời gian t giây thì khối lượng dung dịch giảm 2,715 gam. Giả thiết hiệu suất điện phân là 100%, các khí sinh ra không tan trong nước và nước không bay hơi trong quá trình điện phân. Giá trị của t là
Thứ tự oxh trên anot: Cl- > H2O; thứ tự khử trên catot: Cu2+>H2O
\(\begin{gathered} TN1\left\{ \begin{gathered} BTE:\,\,2{n_{Cu}} + 2{n_{{H_2}}} = 2{n_{C{l_2}}} = \frac{{It}}{F} = 0,04 \hfill \\ {\overline M _{(C{l_2},\,\,{H_2})}} = \frac{{71{n_{C{l_2}}} + 2{n_{{H_2}}}}}{{{n_{C{l_2}}} + {n_{{H_2}}}}} = 48 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} {n_{C{l_2}}} = 0,02 \hfill \\ {n_{{H_2}}} = 0,01 \hfill \\ {n_{Cu}} = 0,01 \hfill \\ \end{gathered} \right. \Rightarrow X\,\,co\`u \,\,\left\{ \begin{gathered} CuS{O_4}:\,\,0,01\,\,mol \hfill \\ KCl:\,\,0,05\,\,mol \hfill \\ \end{gathered} \right\}\, \hfill \\ TH2\,\,\left\{ \begin{gathered} BTE:\,\,2\underbrace {{n_{Cu}}}_{0,01} + 2{n_{{H_2}}} = 2\underbrace {{n_{C{l_2}}}}_{0,025} + 4{n_{{O_2}}} \hfill \\ {m_{dd\,\,giam}} = 64\underbrace {{n_{Cu}}}_{0,01} + 2{n_{{H_2}}} = 71\underbrace {{n_{C{l_2}}}}_{0,025} + 32{n_{{O_2}}} = 2,715 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} {n_{{O_2}}} = 0,0075 \hfill \\ {n_{{H_2}}} = 0,03 \hfill \\ \end{gathered} \right. \hfill \\ \Rightarrow t = \frac{{96500.(0,01.2 + 0,03.2)}}{2} = \boxed{3860\,\,s} \hfill \\ \end{gathered} \)
Đun nóng 0,2 mol hỗn hợp X gồm một este đơn chức và một este hai chức với dung dịch NaOH vừa đủ, thu được một ancol Y duy nhất và 24,52 gam hỗn hợp Z gồm các muối. Dẫn toàn bộ Y qua bình đựng Na dư, thấy khối lượng bình tăng 9,0 gam. Đốt cháy hoàn toàn 24,52 gam Z cần dùng 0,52 mol O2, thu được Na2CO3 và 24,2 gam hỗn hợp gồm CO2 và H2O. Phần trăm khối lượng của muối có khối lượng phân tử lớn nhất trong hỗn hợp Z là
- BTKL → nNa2CO3 = 0,16 → nNaOH = 0,32 → Tỉ lệ 1 < nNaOH/nX < 2 → Este đơn chức của ancol
TH 1: Đều este của ancol
→ nOH (ancol) = nNaOH = 0,32 → mancol = 9 + 0,32 = 9,32 → Mancol = 29,125 (loại)
TH 2: Este 2 chức (1 chức este ancol + 1 chức este phenol)
® nX = 0,14 ; nY = 0,06 ® Snancol = 0,2 ® mancol = 9,2 ® Mancol = 46 (C2H5OH)
*) Tìm muối
3 muối R1COONa: 0,14 ; R2(COONa)2: 0,06 và R3 – C6H4ONa: 0,06
- BTNT O và tổng khối lượng hỗn hợp → nCO2 = 0,46 ; nH2O = 0,22
- BTNT C → 0,14(n + 1) + 0,06(m + 2) + 0,06(p + 6) = 0,46 + 0,16
→ 7n + 3m + 3p = 0 ® n = m = p = 0
→ 3 muối là HCOONa: 0,14 ; (COONa)2: 0,06 ; C6H5ONa: 0,06
→%m(COONa)2 = 32,78956% (B)
Đề thi liên quan
-
Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Lê Lợi
-
40 câu hỏi
-
90 phút
-