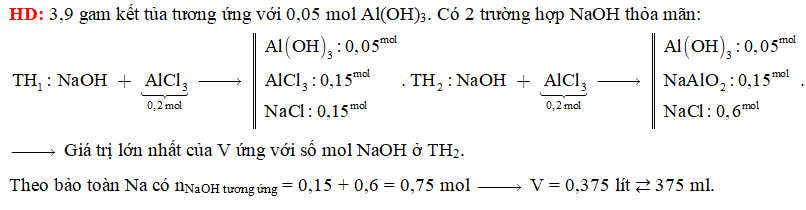Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Phan Đăng Lưu
Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Phan Đăng Lưu
-
Hocon247
-
40 câu hỏi
-
90 phút
-
128 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Phát biểu nào sau đây đúng?
Phản ứng thủy phân chất béo trong môi trường axit hoặc kiềm luôn thu được glixerol.
Ở điều kiện thích hợp, hai chất phản ứng với nhau tạo thành metyl fomat là
Ở điều kiện thích hợp, hai chất phản ứng với nhau tạo thành metyl fomat là HCOOH và CH3OH.
Ở điều kiện thường, kim loại nào sau đây dẫn điện tốt nhất?
Ở điều kiện thường, kim loại Ag dẫn điện tốt nhất
Kim loại nào sau đây là kim loại kiềm thổ ?
Ca là kim loại kiềm thổ
Khí X là sản phẩm chính trong sự cháy không hoàn toàn của cacbon và các hợp chất chứa cacbon.Khí X có độc tính cao, có khả năng liên kết với hemoglobin trong máu làm đông máu. Khí X là
Khí X là CO
Etyl propionat là este có mùi thơm của dứa. Công thức của etyl propionat là
Công thức của etyl propionat là C2H5COOC2H5
Cho dung dịch NaOH vào dung dịch chất X, thu được kết tủa màu nâu đỏ. Lọc kết tủa nung trong không khí đến khối lượng không đổi thu được chất Y có màu đỏ nâu. Chất X là
Chất X là FeCl3
Thủy phân đến cùng các protein đơn giản thu được sản phẩm gồm các
Thủy phân đến cùng các protein đơn giản thu được sản phẩm gồm các aminoaxit.
Al2O3 không tan được trong dung dịch nào sau đây?
Al2O3 không tan được trong dung dịch BaCl2
Poli (vinyl clorua) được điều chế từ phản ứng trùng hợp chất nào sau đây?
Poli (vinyl clorua) được điều chế từ phản ứng trùng hợp chất CH2=CHCl.
Chất nào sau đây thuộc loại đisaccarit?
Saccarozơ thuộc loại đisaccarit
Thạch cao nung dùng để bó bột khi gãy xương, đúc tượng, phấn viết bảng… Công thức hóa học của thạch cao nung là
Công thức hóa học của thạch cao nung là CaSO4.H2O
Cho thanh Fe nặng 100 gam vào 100 ml dung dịch CuSO4 a M. Sau khi phản ứng xảy ra hoàn toàn, lấy thanh sắt ra sấy nhẹ làm khô thì thấy khối lượng thanh sắt tăng thêm 1,6 gam. Giá trị của a là
Giá trị của a là 2
Cho các chất sau: metylamin, alanin, metylamoni clorua, phenol. Số chất phản ứng được với dung dịch NaOH là
Số chất phản ứng được với dung dịch NaOH là alanin, metylamoni clorua, phenol
Lên men m gam glucozơ thành ancol etylic với hiệu suất 60%. Toàn bộ khí CO2 sinh ra được hấp thụ vào dung dịch nước vôi trong dư, thu được 80 gam kết tủa. Giá trị của m là
nCO2 = nCaCO3 = 0,8 mol
C6H12O6 → 2C2H5OH + 2CO2
0,4 ← 0,8 (mol)
=> mglu lí thuyết = 0,4.180 = 72 (g)
Vì H = 60% => lượng glu cần lấy = 72 : 0,6 = 120 (g)
Đốt cháy hoàn toàn amin X (no, đơn chức, mạch hở), thu được 0,4 mol CO2 và 0,05 mol N2. Công thức phân tử của X là
Công thức phân tử của X là C4H11N
Phản ứng nào sau đây có phương trình ion rút gọn là: Ba2+ + SO42- → BaSO4?
BaCl2 + Na2SO4 → BaSO4 +2NaCl
Thủy phân hoàn toàn tinh bột, thu được monosaccarit X. Hiđro hóa X, thu được chất hữu cơ Y. Hai chất X, Y lần lượt là:
Thủy phân hoàn toàn tinh bột, thu được monosaccarit X. Hiđro hóa X, thu được chất hữu cơ Y. Hai chất X, Y lần lượt là: glucozơ,sobitol
Tiến hành các thí nghiệm sau:
(1) Nhúng thanh đồng nguyên chất vào dung dịch FeCl3.
(2) Cắt miếng sắt tây (sắt tráng thiếc), để trong không khí ẩm.
(3) Nhúng thanh kẽm vào dung dịch H2SO4 loãng có nhỏ vài giọt dung dịchCuSO4.
(4) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc nước muối.
(5) Đốt dây Fe trong khí clo
Trong các thí nghiệm trên, số thí nghiệm chỉ xảy ra ăn mòn hóa học là
Phát biểu đúng là f, j
: Thủy phân este mạch hở X có công thức phân tử C4H6O2, thu được sản phẩm đều có phản ứng tráng bạc. Số công thức cấu tạo phù hợp của X là
Đáp án D ( 1 công thức HCOOCH=CHCH3 )
Cho các chất sau: CrO3, Fe, Cr(OH)3, Cr, Al(OH)3, Fe2O3. Số chất tan được trong dung dịch NaOH là
Số chất tan được trong dung dịch NaOH là CrO3,Cr(OH)3, Al(OH)3
Cho các polime: poli(vinyl clorua), xenlulozơ, tơ tằm, cao su buna, xenlulozơ triaxetat, nilon-6,6, tơ nitron. Số polime tổng hợp là
Số polime tổng hợp là poli(vinyl clorua), tơ nitron.
Dẫn 6,72 lít khí CO (đktc) qua m gam hỗn hợp gồm Fe2O3 và MgO (tỉ lệ mol 1 : 1) nung nóng, thu được hỗn hợp khí có tỉ khối hơi so với He bằng 10,2. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
\(\left\{ \begin{gathered} CO:{0,06^{mol}} \hfill \\ C{O_2}:{0,24^{mol}} \hfill \\ \end{gathered} \right. \to m = \frac{{0,24}}{3}.(160 + 40) = 16{\text{ gam}}\)
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 4,83 gam O2, thu được 3,42 mol CO2 và 3,18 mol H2O. Mặt khác, cho a gam X phản ứng vừa đủ với dung dịch NaOH, thu được b gam muối. Giá trị của b là
\(\xrightarrow{{BTKL}}{m_X} = 44{n_{C{O_2}}} + 18{n_{{H_2}O}} - 32{n_{{O_2}}} = 53,16\,(g)\xrightarrow{{BT:\,O}}{n_X} = \frac{{2{n_{C{O_2}}} + {n_{{H_2}O}} - 2{n_{{O_2}}}}}{6} = 0,06\;mol\)
Khi cho X tác dụng với NaOH thì : \({n_{NaOH}} = 3{n_X} = 3{n_{{C_3}{H_5}{{(OH)}_3}}} = 0,18\;mol\)
\(\xrightarrow{{BTKL}}{m_{muo i}} = {m_X} + 40{n_{NaOH}} - 92{n_{{C_3}{H_5}{{(OH)}_3}}} = 54,84\,(g)\)
Chất X có công thức phân tử C9H16O4. Khi cho X tác dụng với NaOH dư thu được một muối mà từ muối này điều chế trực tiếp được axit dùng để sản xuất tơ nilon-6,6. Số công thức cấu tạo thoả mãn X là?
Số công thức cấu tạo thoả mãn X là 3
Thực hiện các thí nghiệm sau:
(a) Cho Cu tác dụng với hỗn hợp NaNO3 và HCl.
(b) Cho FeO vào dung dịch H2SO4 đặc, nóng(dư).
(c)Sục khí CO2 vào dung dịch Ca(OH)2dư.
(d)Cho dung dịch KHSO4 vào dung dịchNaHCO3.
(e)Cho dung dịch Fe(NO3)2 vào dung dịch HCl loãng.
(f)Cho đinh sắt vào dung dịch H2SO4 loãng.
(g)Cho Na tác dụng với dung dịch CuSO4
Sau khi các phản ứng xảy ra, số thí nghiệm sinh ra chất khí là
Sau khi các phản ứng xảy ra, số thí nghiệm sinh ra chất khí là
(a) Cho Cu tác dụng với hỗn hợp NaNO3 và HCl.
(b) Cho FeO vào dung dịch H2SO4 đặc, nóng(dư).
(d)Cho dung dịch KHSO4 vào dung dịchNaHCO3.
(e)Cho dung dịch Fe(NO3)2 vào dung dịch HCl loãng.
(f)Cho đinh sắt vào dung dịch H2SO4 loãng.
(g)Cho Na tác dụng với dung dịch CuSO4
Cho các thí nghiệm sau:
(1) Cho hỗn hợp Na và Al (tỉ lệ mol 2 : 1) vào nước dư.
(2) Cho CrO3 vào nước dư.
(3) Vôi sống (CaO) và sođa (Na2CO3) (tỉ lệ mol 1 : 1) vào nước dư.
(4) Cho a mol hỗn hợp Fe2O3 và Cu (tỉ lệ mol 1 : 1) vào dung dịch chứa 3a mol HCl.
(5) Cho a mol khí CO2 vào dung dịch chứa 2a mol NaOH.
(6) Cho a mol Na vào dung dịch chứa a mol CuSO4.
Số thí nghiệm sau khi các phản ứng xảy ra hoàn toàn, phần dung dịch thu được chứa hai chất
Số thí nghiệm sau khi các phản ứng xảy ra hoàn toàn, phần dung dịch thu được chứa hai chất : 1, 2, 4, 6
Cho 112,5 ml ancol etylic 92° tác dụng với Na dư, đến phản ứng hoàn toàn thu được V lít H2 (đktc). Giá trị của V là (biết khối lượng riêng của rượu nguyên chất là 0,8 g/ml và của nước là 1 g/ml):
\(V = 22,4.\left( {\frac{{112,5.0,92.0,8}}{{46.2}} + \frac{{112,5.1.0,08}}{{18.2}}} \right) = 25,76\)
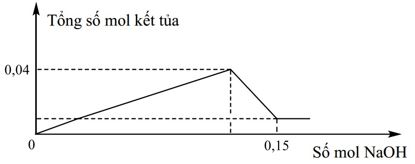
Cho từ từ dung dịch NaOH 0,5M vào 100 ml dung dịch FeCl3 aM và AlCl3 bM, thấy xuất hiện kết tủa, khi kết tủa cực đại thì sau đó kết tủa bị hòa tan một phần. Đồ thị biểu diễn mối quan hệ giữa số mol kết tủa và số mol NaOH cho vào như hình vẽ:
Giá trị của a và b lần lượt là
\(\left\{ \begin{gathered} 0,1a + 0,1b = 0,04 \hfill \\ 0,1a.3 + 0,1b.4 = 0,15 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} a = 0,1 \hfill \\ b = 0,3 \hfill \\ \end{gathered} \right.\)
Cho các phát biểu sau:
(a) Dầu mỡ sau khi sử dụng, có thể tái chế thành nhiên liệu.
(b) Muối mononatri của axit glutamic được dùng làm bột ngọt (mì chính).
(c) Amilopectin, tơ tằm, lông cừu là polime thiên nhiên.
(d) Thủy phân vinyl fomat thu được hai sản phẩm đều có phản ứng tráng bạc.
(e) Khi cho giấm ăn (hoặc chanh) vào sữa bò hoặc sữa đậu nành thì thấy có kết tủa xuất hiện.
(g) Thành phần chính của khi biogas là metan.
Số phát biểu đúng là
Các phát biểu trên đều đúng
Cho 86,3 gam hỗn hợp X gồm Na, K, Ba và Al2O3 (trong đó oxi chiếm 19,47% về khối lượng) tan hết vào nước, thu được dung dịch Y và 13,44 lít khí H2 (đktc). Cho 3,2 lít dung dịch HCl 0,75M vào dung dịch Y. Sau khi các phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m gần nhất với
- Bơm 0,6 mol O vào X
\( \to Y\left\{ \begin{gathered} KL \hfill \\ AlO_2^ - :{0,7^{mol}} \hfill \\ O{H^ - }:0,6.2 - 0,7 = {0,5^{mol}} \hfill \\ \end{gathered} \right. \to {n_ \downarrow } = \frac{{4.0,7 - 2,4 + 0,5}}{3} = 0,3mol \to m = 23,4{\text{ gam}}\)
Cho ba dung dịch X, Y, Z thỏa mãn các tính chất sau:
- X tác dụng với Y tạo kết tủa; - Y tác dụng với Z tạo kết tủa;
- X tác dụng với Z có khí thoát ra.
Các dung dịch X, Y, Z lần lượt là:
Các dung dịch X, Y, Z lần lượt là: \(NaHC{O_3},Ba{(OH)_2},KHS{O_4}.\)
Hỗn hợp E gồm bốn este đều có công thức C8H8O2 và có vòng benzen. Cho 16,32 gam E tác dụng tối đa với V ml dung dịch NaOH 1M (đun nóng), thu được hỗn hợp X gồm các anool và 18, 78 gam hỗn hợp muối. Cho toàn bộ X vào bình đựng kim loại Na dư, sau khi phản ứng kết thúc khối lượng chất rắn trong bình tăng 3,83 gam so với ban đầu. Giá trị của V là
\(\left\{ \begin{gathered} est{e_{ancol}}:{x^{mol}} \hfill \\ est{e_{phenol}}:{y^{mol}} \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x + y = 0,12 \hfill \\ 16,32 + 40(x + 2y) = 18,78 + 3,83 + x + 18y \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x = 0,05 \hfill \\ y = 0,07 \hfill \\ \end{gathered} \right.\)
\( \to V = \frac{{0,05 + 0,07.2}}{1} = 0,19\)
Tiến hành thí nghiệm xà phòng hóa tristearin theo các bước sau:
Bước 1: Cho vào bát sứ khoảng 1 gam tristearin và 2 – 2,5 ml dung dịch NaOH nồng độ 40%.
Bước 2: Đun sôi nhẹ hỗn hợp khoảng 30 phút và khuấy liên tục bằng đũa thủy tinh, thỉnh thoảng thêm vài giọt nước cất để giữ cho thể tích của hỗn hợp không đổi.
Bước 3: Rót thêm vào hỗn hợp 4 – 5 ml dung dịch NaCl bão hòa nóng, khuấy nhẹ rồi để nguội.
Phát biểu nào sau đây sai?
A. Đúng, Sau bước 3, thấy có lớp chất rắn màu trắng nhẹ nổi lên trên bề mặt của chất lỏng đó là xà phòng và phần chất lỏng ở dưới là NaCl và glixerol.
B. Đúng, Sau bước 2, các chất được tạo thành sau phản ứng xà phòng hoá hoà tan với nhau nên lúc này trong bát sứ thu được chất lỏng đồng nhất.
C. Sai, Mục đích chính của việc thêm dung dịch NaCl bão hoà là để kết tinh xà phòng lên trên bề mặt chất lỏng.
D. Đúng, Sau bước 3, chất lỏng trong ống nghiệm có chứa glixerol hoà tan được Cu(OH)2 thành dung dịch có màu xanh lam.
X và Y là hai axit cacboxylic hai chức, mạch hở kế tiếp nhau trong dãy đồng đẳng; Z và T là hai este thuần chức hơn kém nhau 14 đvC, đồng thời Y và Z là đồng phân của nhau (MX < MY< MT). Đốt cháy hoàn toàn 17,28 gam hỗn hợp E chứa X, Y, Z, T cần dùng 10,752 lít oxi (ở đktc). Mặt khác 17,28 gam hỗn hợp E tác dụng vừa đủ với 300 ml dung dịch NaOH 1M thu được 4,2 gam hỗn hợp 3 ancol có cùng số mol. Số mol của X trong E là
\(\left\{ \begin{gathered} C{O_2}:{x^{mol}} \hfill \\ {H_2}O:{y^{mol}} \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} \xrightarrow{{BT{\text{ O}}}}2x + y = 0,3.2 + 0,48.2 \hfill \\ 44x + 18y = 32,64 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x = 0,57 \hfill \\ y = 0,42 \hfill \\ \end{gathered} \right.\)
\({n_{C{O_2}}} - {n_{{H_2}O}} = {n_X} \to \)
Các chất trong E đều no, hai chức, mạch hở
\(\xrightarrow{{Lam{\text{ troi}}}}\left\{ \begin{gathered} Z:{(COO)_2}{C_2}{H_4}:{a^{mol}} \hfill \\ T:C{H_3}OOC - COO{C_2}{H_5}:{b^{mol}} \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} a = b \hfill \\ 62a + 32b + 46b = 4,2 \hfill \\ \end{gathered} \right. \to a = b = 0,03\)
\(\left\{ \begin{gathered} {n_X} + {n_Y} = 0,15 - 0,06 = 0,09 \hfill \\ 3{n_X} + 4{n_Y} = 0,57 - 0,03.4 - 0,03.5 = 0,3 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} {n_X} = 0,06mol \hfill \\ {n_Y} = 0,03mol \hfill \\ \end{gathered} \right.\)
Hòa tan hoàn toàn 21,5 gam hỗn hợp X gồm Al, Zn, FeO, Cu(NO3)2 cần dùng hết 430 ml dung dịch H2SO4 1M thu được 0,19 mol hỗn hợp khí Y (đktc) gồm hai khí không màu, có 1 khí hóa nâu ngoài không khí, có tỉ khối hơi so với H2 bằng 5,421; dung dịch Z chỉ chứa các muối sunfat trung hòa. Cô cạn dung dịch Z thu được 56,9 gam muối khan. Phần trăm khối lượng của Al trong hỗn hợp X có giá trị gần giá trị nào nhất?
\(Y\left\{ \begin{gathered} {H_2}:{0,13^{mol}} \hfill \\ NO:{0,06^{mol}} \hfill \\ \end{gathered} \right.\xrightarrow{{BTKL}}{n_{{H_2}O}} = {0,26^{mol}}\xrightarrow{{{H^ + }}}{n_{NH_4^ + }} = {0,02^{mol}}\xrightarrow{{BT{\text{ N}}}}{n_{Cu{{(N{O_3})}_2}}} = {0,04^{mol}}\)
\(\xrightarrow{{{H^ + }}}{n_O} = {n_{FeO}} = {0,08^{mol}}\)
\(\left\{ \begin{gathered} Al:{x^{mol}} \hfill \\ Zn:{y^{mol}} \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} 27x + 65y + 0,08.72 + 0,04.188 = 21,5 \hfill \\ \xrightarrow{{BTe}}3x + 2y = 0,6 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x = 0,16 \hfill \\ y = 0,06 \hfill \\ \end{gathered} \right. \to \% {m_{Al}} = 20,09\% \)
Cho hỗn hợp X gồm một tetrapeptit và một tripeptit. Để thủy phân hoàn toàn 50,36 gam X cần dung dịch chứa 0,76 mol NaOH, sau phản ứng hoàn toàn cô cạn thu được 76,8 gam hỗn hợp muối chỉ gồm a mol muối glyxin và b mol muối alanin. Mặt khác đốt cháy hoàn toàn 0,11 mol X bằng O2 dư thu được m gam CO2. Giá trị của m là
\(\xrightarrow{{BTKL}}{n_{{H_2}O}} = {n_X} = {0,22^{mol}}\)
\(\left\{ \begin{gathered} GlyNa:{x^{mol}} \hfill \\ AlaNa:{y^{mol}} \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x + y = 0,76 \hfill \\ 97x + 111y = 76,8 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x = 0,54 \hfill \\ y = 0,22 \hfill \\ \end{gathered} \right.\)
\(m = \frac{{0,54.2 + 0,22.3}}{2}.44 = 38,28{\text{ gam}}\)
Đề thi liên quan
-
Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Phan Đăng Lưu
-
40 câu hỏi
-
90 phút
-