Đề thi thử THPT QG môn Hóa học năm 2018 - Trường THPT Chuyên ĐH Sư Phạm- Lần 2
Đề thi thử THPT QG môn Hóa học năm 2018 - Trường THPT Chuyên ĐH Sư Phạm- Lần 2
-
Hocon247
-
40 câu hỏi
-
90 phút
-
63 lượt thi
-
Dễ
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Nước thải công nghiệp thường chứa các ion kim loại nặng như Hg2+, Pb2+, Fe3+, … Để xử lí sơ bộ nước thải trên, làm giảm nồng độ các ion kim loại nặng với chi phí thấp, người ta sử dụng chất nào sau đây?
Đáp án C
Dùng Ca(OH)2 để kết tủa hết các kim loại nặng
Hg2+ + 2OH- → Hg(OH)2↓
Pb2+ + 2OH- → Pb(OH)2↓
Fe3+ + 3OH- → Fe(OH)3↓
Hỗn hợp X gồm Mg ( 0,10 mol); Al ( 0,04 mol) và Zn ( 0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng ( dư), sau phản ứng khối lượng dung dịch tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là
Đáp án A
mKL = 0,1.24 + 0,04.27 + 0,15.65 = 13,23 (g) đúng bằng khối lượng dung dịch tăng
=> KL + HNO3 chỉ tạo muối NH4+
=> nNH4+ = 1/8 ne(KL nhường) = 1/ 8 . ( 0,1.2 + 0,04.3 + 0,15.2) = 0,0775 (mol)
=> nHNO3 PƯ = 10nNH4+ = 0,775 (mol)
Xét sơ đồ phản ứng ( trong dung dịch) giữa các hợp chất hữu cơ:
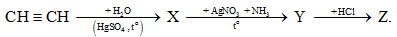
Công thức của Z là
X là CH3-CHO
Y là CH3COONH4
Z là CH3COOH
Kim loại có khối lượng riêng nhỏ nhất là
Đáp án D
Li là kim loại có khối lượng riêng nhỏ nhất
Cho sơ đồ điều chế HNO3 trong phòng thí nghiệm
Phát biểu nào sau đây là sai khi nói về quá trình điều chế HNO3?
Đáp án B
A,C, D đúng
B sai vì HNO3 là axit mạnh, bị đẩy ra khỏi dung dịch muối do tính dễ bay hơi của HNO3
Cho phản ứng: aFe + bHNO3 → cFe(NO3)3 + dNO + eH2O
Các hệ số a, b, c, d, e là những số nguyên đơn giản nhất. Tổng ( a+ b) bằng:
Đáp án B
PTHH: Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
=> a+ b = 1+ 4 = 5
Thủy phân 342 gam tinh bột với hiệu suất của phản ứng là 75%, khối lượng glucozơ thu được
Đáp án C
(C6H10O5)n → nC6H12O6
ntb = 324 : 162 = 2 (mol)
=> nglu = 2 (mol)
Vì H = 75% => mglu = ( 2. 180).0,75 = 270 (g)
Thủy phân 4,4 gam etyl axetat bằng 100ml dung dịch NaOH 0,2M. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được m gam chất rắn khan. Giá trị của m là
Đáp án D
nCH3COOC2H5 = 4,4 : 88 = 0,05 (mol) ; nNaOH = 0,02 (mol)
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
0,02← 0,02 →0,02
mRẮN = mCH3COONa = 0,02. 82 = 1,64 (g)
Cho 4,4 gam một anđehit no, đơn chức, mạch hở X phản ứng hoàn toàn với một lượng dư dung dịch AgNO3 trong NH3 đun nóng thu được 21,6 gam kim loại Ag. Công thức của X là
Đáp án D
nAg = 21,6 : 108 = 0,2 (mol)
=> nRCHO = nAg/2 = 0,1 (mol)
=> MRCHO = 4,4 : 0,1 = 44 (g/mol) => CH3CHO
Đốt cháy hoàn toàn hỗn hợp metyl axetat và etyl axetat, thu được CO2 và m gam H2O. Hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 dư, thu được 25 gam kết tủa. Giá trị của m là
Đáp án A
Đốt cháy metyl axetat và etyl axetat đều thu được nCO2 = nH2O
=> nH2O = nCO2 = nCaCO3 = 25: 100 = 0,25 (mol)
=> mH2O = 0,25. 18 = 4,5 (g)
Để phân biệt dung dịch AlCl3 và dung dịch KCl ta dùng dung dịch
Đáp án C
Dùng dd NaOH để phân biệt AlCl3 và KCl vì khi cho từ từ đến dư dd NaOH vào AlCl3 có hiện tượng xuât hiện kêt tủa sau đó kết tủa tan, còn KCl thì không có hiện tượng gì
AlCl3 + 3NaOH → 3NaCl + Al(OH)3↓
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Có các nhận xét sau:
(a) Phân đạm amoni không nên bón cho loại đất chua.
(b) Độ dinh dưỡng của phân lân được đánh giá bằng phần trăm khối lượng photpho.
(c) Thành phần chính của supephotphat kép là Ca(HPO4)2. CaSO4.
(d) Người ta dùng loại phân bón chứa nguyên tố kali để tăng cường sức chống bệnh, chống rét và chịu hạn cho cây.
(e) Tro thực vật cũng là một loại phân kali vì có K2CO3.
(f) Amophot là một loại phân bón phức hợp.
Số nhận xét sai là
Đáp án C
Các nhận xét sai:
b) sai vì độ dinh dưỡng của phân lân được đánh giá bằng phần trăm khối lượng P2O5
c) sai vì thành phần chính của supephotphat kép là Ca(H2PO4)2.
=> Có 2 nhận xét sai
Tên gọi của polime có công thức (-CH2-CH2-)n là
Tên gọi của polime có công thức (-CH2-CH2-)n là polietilen.
Đáp án A
Cho các chất sau: etyl axetat, tripanmitin, saccarozơ, etylamin, Gly- Ala. Số chất tham gia phản ứng thủy phân trong môi trường kiềm là
Đáp án C
Các chất thủy phân trong môi trường kiềm: etyl axetat, tripanmitin, Gly- Ala => có 3 chất
Thủy phân este X trong môi trường kiền, thu được natri axetat và rượu etylic. Công thức của X là
Đáp án A
X là: CH3COOC2H5
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
Tơ được sản xuất từ xenlulozo là
Đáp án B
Tơ visco là tơ được sản xuất từ xenlulozo
Chất nào sau đây là chất điện li yếu?
Đáp án D
Ghi nhớ: Chất điện li yếu là các axit yếu, bazo yếu
Trong thực tế, không sử dụng cách nào sau đây để bảo vệ kim loại sắt khỏi bị ăn mòn?
Đáp án B
Để bảo vệ sắt bị ăn mòn thì phải phủ một kim loại hoạt động hóa học hơn sắt lên bề mặt của sắt
=> phủ đồng là kim loại yếu hơn sắt nên sắt thì sẽ không bảo vệ được sắt
Đốt cháy hoàn toàn amin X ( nơ, đơn chức, mạch hở) bằng O2, thu được 4,48 lít CO2 và 1,12 lít N2 ( các thể tích khí đo ở đktc). Công thức phân tử của X là
Đáp án B
nCO2 = 4,48 : 22,4 = 0,2 (mol); nN2 = 1,12 : 22,4 = 0,05 (mol)
Gọi CTCT của amin là CnH2n+3 N
BTNT N: namin = 2nN2 = 0,1 (mol)
n = nCO2/ namin = 0,2 : 0,1 = 2
=> CTPT C2H7N
Phát biểu nào sau đây đúng?
Đáp án A
A. đúng vì C6H5NH2 + HCl → C6H5NH3Cl ( muối không độc)
B. sai, các amin là các chất độc
C. sai, các amin đầu thì dễ tan trong nước, các amin tiếp theo khó tan hơn, riêng anilin rất ít tan trong nước.
D. sai, anilin không làm quỳ tím chuyển màu
Hấp thụ hoàn toàn 4,48 lít khí SO2 ( ở đktc) vào dung dịch chứa 16 gam NaOH, thu được dung dịch X. Khối lượng muối tan thu được trong dung dịch X là
Đáp án D
nSO2 = 4,48 : 22,4 = 0,2 (mol) ; nNaOH = 16: 40 = 0,4 (mol)
Ta thấy nNaOH/ nSO2 = 2 => chỉ tạo muối Na2SO3
=> mNa2SO3 = 0,2. 126 = 25, 2(g)
Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl ( điện cực trơ), thu được khí H2 ở catot.
(b) Cho CO dư qua hỗn hợp Al2O3 và CuO đun nóng, thu được Al và Cu.
(c) Nhúng thanh Zn vào dung dịch chứa CuSO4 và H2SO4, có xuất hiện ăn mòn điện hóa.
(d) Kim loại có nhiệt độ nóng chảy thấp nhất là Hg, kim loại dẫn điện tốt nhất là Ag.
(e) Cho dung dịch AgNO3 dư vào dung dịch FeCl2, thu được chất rắn gồm Ag và AgCl.
Số phát biểu đúng là
Các phát biểu đúng là: a)
a) đúng vì 2NaCl + 2H2O → 2NaOH + H2 (catot) + Cl2 (anot)
b) sai CO không khử được Al2O3 nên sau phản ứng phải thu được Al2O3 và Cu
c) đúng
d) đúng
e) đúng 3AgNO3 + FeCl2 → Fe(NO3)3 + 2AgCl↓ + Ag↓
→ có 4 phát biểu đúng
Alinin ( C6H5NH2) và phenol (C6H5OH) đều có phản ứng với
Anilin (C6H5NH2) và phenol (C6H5OH) đều có phản ứng với dung dịch Br2 tạo kết tủa trắng
Điện phân nóng chảy hoàn toàn 5,96 gam MCln, thu được 0,04 mol Cl2. Kim loại M là
2MCln → 2M + nCl2
0,08/n ← 0,04 (mol)
Ta có:
\(\frac{{0,08}}{n}(M + 35,5n) = 5,96 \to M = 39n\)
→ n = 1 thì M =39 (Kali)
Cho 66,2 gam hỗn hợp X gồm Fe3O4, Fe(NO3)2, Al tan hoàn toàn trong dung dịch chứa 3,1 mol KHSO4. Sau phản ứng hoàn toàn thu được dung dịch Y chỉ chứa 466,6 gam muối sunphat trung hòa và 10,08 lít đktc khí Z gồm 2 khí trong đó có một khí hóa nâu ngoài không khí. Biết tỷ khối của Z so với He là 23182318. Phần trăm khối lượng của Al trong hỗn hợp X gần nhất với giá trị nào sau đây?
M khí = 4.23/18 = 46/9 → Khí có chứa H2
Thành phần của khí: NO (x mol) và H2 (y mol)
n khí = x + y = 0,45 (1)
m khí = 30x + 2y = 0,45.46/9 (2)
Từ (1) (2) → x = 0,05 và y = 0,4
Sơ đồ bài toán:
\(66,2(g)\left\{ \begin{array}{l}
F{e_3}{O_4}\\
Fe{(N{O_3})_2}\\
Al
\end{array} \right. + KHS{O_4}:3,1 \to 466,6(g)\left\{ \begin{array}{l}
F{e^{2 + }}\\
F{e^{3 + }}\\
A{l^{3 + }}\\
{K^ + }:3,1\\
N{H_4}^ + \\
S{O_4}^{2 - }:3,1
\end{array} \right. + \left\{ \begin{array}{l}
NO:0,05\\
{H_2}:0,4
\end{array} \right. + {H_2}O\)
BTKL: mH2O = mX + mKHSO4 – m khí = 66,2 + 3,1.136 – 466,6 – 0,05.30 – 0,4.2 = 18,9 gam → nH2O = 1,05 mol
BTNT “H”: nNH4+ = (nKHSO4 – 2nH2 – 2nH2O) : 4 = (3,1 – 2.0,4 – 2.1,05) : 4 = 0,05 mol
→ m(Fe, Al) = m muối – mK+ – mNH4+ - mSO42- = 466,6 – 3,1.39 – 0,05.18 – 3,1.96 = 47,2 gam
Mặt khác, BTNT “N”: nFe(NO3)2(X) = (nNH4+ + nNO) : 2 = (0,05 + 0,05) : 2 = 0,05 mol
mO(X) = mX – m(Fe, Al) – mNO3- = 66,2 – 47,2 – 0,1.62 = 12,8 gam → nO = 0,8 mol
→ nFe3O4 = nO : 4 = 0,2 mol
→ mAl = mX – mFe3O4 – mFe(NO3)2 = 66,2 – 0,2.232 – 0,05.180 = 10,8 gam
→ %mAl = 10,8 : 66,2 = 16,3% gần nhất với 15%
Đun nóng 48,2 g hỗn hợp KMnO4, KClO3, sau một thời gian thu được 43,4 gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, sau phản ứng thu đc 15,12 lít Cl2 (đktc) và dung dịch gồm MnCl2, KCl, HCl dư. Số mol HCl phản ứng là
Đáp án D
Đặt a, b là số mol KMnO4 và KClO3 ban đầu
=> 158a + 122,5b = 48,2 (1)
nO (X) = 4a + 3b
=> nO(Y) = 4a + 3b – 0,3
=> nHCl = 2nH2O = 2 (4a + 3b – 0,3)
Dung dịch thu được chứa KCl ( a + b) ; MnCl2 ( a)
Bảo toàn nguyên tố Cl: b + 2( 4a + 3b – 0,3) = a + b + 2a + 2.0,675 (2)
Từ ( 1) và (2) => a = 0,15 và b = 0,2
=> nHCl = 1,8 mol
Hỗn hợp X gồm hai muối R2CO3 và RHCO3. Chia 44,7 gam X thành ba phần bằng nhau:
- Phần một tác dụng hoàn toàn với dung dịch Ba(OH)2 dư, thu được 35,46 gam kết tủa.
- Phần hai tác dụng hoàn toàn với dung dịch BaCl2 dư, thu được 7,88 gam kết tủa.
- Phần ba tác dụng tối đa với V ml dung dịch KOH 2M.
Giá trị của V là
Đáp án A
Gọi số mol R2CO3 và RHCO3 lần lượt là x và y mol trong mỗi phần
+ Phần 1: nBaCO3 = x + y = 0,18 mol
+ Phần 2: nBaCO3 = x = 0,04 mol => y = 0,14 mol
Vậy xét trong mỗi phần có m = 14,9 g
=> 0,04. ( 2R + 60) + 0,14. ( R + 61) = 14,9
=> R = 18 ( NH4)
+ Phần 3: nKOH = 2nNH4HCO3 + 2n(NH4)2CO3 = 0,36 mol
=> V = 0,18 lít = 180ml
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch có pH là
Đáp án A
∑ nH+ = 2nH2SO4 + nHCl = 2. 0,1.0,05 + 0,1.0,1 = 0,02 (mol)
∑ nOH- = nNaOH + 2nBa(OH)2 = 0,1.0,2 + 2. 0,1.0,1 = 0,04 (mol)
H+ + OH- → H2O
0,02 → 0,02
=> nOH- dư = 0,04 – 0,02 = 0,02 (mol)
=> [OH-] = n: V = 0,02 : 0,2 = 0,01 M
pH = 14 + log(OH-) = 14 + (-1) = 13
Tiến hành thí nghiệm với các dung dịch X, Y, Z, và T. Kết quả được ghi ở bảng sau;
Đáp án D
X phản ứng với dd AgNO3/NH3 cho ra kết tủa Ag=> X là etyl fomat
Y làm quỳ tím chuyển sang màu xanh => Y là lysin ( có 2 nhóm NH2)
Z vừa tạo kết tủa Ag với dd AgNO3/NH3 vừa tạo dung dịch xanh lam với Cu(OH)2 => Z là glucozo
T tạo kết tủa trắng với dd Br2 => T là anilin hoặc phenol
Vậy thứ tự phù hợp X, Y, Z, T là etyl fomat, lysin, glucozo, phenol
Cho m gam bột Fe vào 200 ml dung dịch chứa hai muối AgNO3 0,15M và Cu(NO3)2 0,1M, sau một thời gian thu được 3,84 gam hỗn hợp kim loại và dung dịch X. Cho 3,25 gam bột Zn vào dung dịch X, sau khi phản ứng xảy ra hoàn toàn, thu được 3,895 gam hỗn hợp kim loại và dung dịch Y. Giá trị của m là
Khi cho X vào dung dịch chứa 0,03 mol AgNO3 và 0,02 mol Cu(NO3)2
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Cu(NO3)2 + Fe → Fe(NO3)2 + Cu
Khi cho Zn vào thì
nZn = 0,05 mol > → Sau phản ứng này Zn còn dư
nZn dư = 0,05 – 0,035 = 0,015 mol
Ta có
Sau phản ứng có mkim loại = mrắn (1) + mrắn (2) + mZn(Y) = 3,84 + 3,895 + 0,035.65 = 10,01
Bảo toàn khối lượng có m + 7,77 = 10,01
→ m = 2,24 g
Hỗn hợp E gồm 2 este đơn chức, là đồng phân cấu tạo và đều chứa vòng benzen. Đốt cháy hoàn toàn m gam E cần vừa đủ 8,064 lít khí O2 (đktc), thu được 14,08 gam CO2 và 2,88 gam H2O. Đun nóng m gam E với dung dịch NaOH (dư) thì có tối đa 2,80 gam NaOH phản ứng, thu được dung dịch T chứa 6,62 gam hỗn hợp 3 muối. Khối lượng của axit cacboxylic trong T là
Ta có:
nCO2 = 0,32, nH2O = 0,16 và nO2 = 0,36 → nO trong E = 0,08 mol
→ nE = 0,04 mol
- Bảo toàn khối lượng: m = 0,32.12 + 0,16.2+ 0,08.16 = 5,44g
- Ta có: nC : nH : nO = 0,32 : 0,32: 0,08 = 4:4:1
- E đơn chức → CTPT của E là C8H8O2
- Sau phản ứng thủy phân thu được 3 muối → có 1 este của phenol
Gọi este của phenol là A có x mol, este của ancol là B có y mol
Ta có hệ phương trình
nE = x + y = 0,04 và nNaOH = 2x+ y = 0,07
→ x = 0,03 và y = 0,01
este của phenol:
Ví dụ HCOOC6H4CH3 hoặc CH3COOC6H5 tác dụng với sẽ thu được muối của axit cacboxylic, muối của phenol và H2O
este của ancol: có thể là C6H5COOCH3 hoặc HCOOCH2C6H5, tác dụng với NaOH sẽ thu được muối của axit cacboxylic và ancol ROH
Bảo toàn khối lượng có mROH = 1,08 g → MROH = 108 → ROH là C6H5CH2OH
Tổng m muối trong T = mHCOONa + mCH3COONa = 3,14 gam
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 4,83 mol O2, thu được 3,42 mol CO2 và 3,18 mol H2O. Mặt khác, cho a gam X phản ứng vừa đủ với dung dịch NaOH, thu được b gam muối. Giá trị của b là
*Phản ứng cháy:
BTKL: mX = mCO2 + mH2O – mO2 = 3,42.44 + 3,18.18 – 4,83.32 = 53,16 gam
BTNT “O”: nO(X) = 2nCO2 + nH2O – 2nO2 = 3,42.2 + 3,18 – 4,83.2 = 0,36 mol
→ nX = nO(X) : 6 = 0,36 : 6 = 0,06 mol
*Phản ứng thủy phân trong NaOH:
X + 3NaOH → Muối + C3H5(OH)3
nNaOH = 3nX = 0,06.3 = 0,18 mol
nGlixerol = nX = 0,06 mol
BTKL: m muối = mX + mNaOH – mglixerol = 53,16 + 0,18.40 – 0,06.92 = 54,84 gam
Cho sơ đồ chuyển hóa sau:
Biết X là axit glutamic, Y, Z, T là các chất hữu cơ chứa nitơ. Công thức phân tử của Y và T là
X là C5H9O4N
Y là C6H12O4NCl
Z là C8H16O4NCl
T là C5H7O4Na2N
Hỗn hợp T gồm hai ancol đơn chức X và Y (MX
\(\begin{gathered}
2\overline R OH\xrightarrow{{H2SO4dac,140oC}}\overline R {\text{O}}\overline {\text{R}} + {H_2}O \hfill \\
{M_{\overline R {\text{O}}\overline {\text{R}} }} = \frac{{6,76}}{{0,08}} = 84,5 \to 2\overline R + 16 = 84,5 \hfill \\
\to 29({C_2}{H_5} - ) < \overline R = 34,25 < 43({C_3}{H_7} - ) \hfill \\
\end{gathered} \)
Đốt Z cũng như đốt T:
\(\begin{gathered}
\left\{ \begin{gathered}
{C_2}{H_5}OH:x \hfill \\
{C_3}{H_7}OH:y \hfill \\
\end{gathered} \right. \to 46x + 60y = 27,2(1) \hfill \\
{C_2}{H_6}O + 3{O_2} \to 2C{O_2} + 3{H_2}O \hfill \\
x\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,3x \hfill \\
{C_3}{H_8}O + 4,5{O_2} \to 3C{O_2} + 4{H_2}O \hfill \\
y\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,4,5y \hfill \\
\to {n_{{O_2}}} = 3x + 4,5y = 1,95(2) \hfill \\
\xrightarrow{{(1)(2)}}x = 0,2;y = 0,3 \hfill \\
\end{gathered} \)
Phản ứng ete hóa: Gọi số mol C2H5OH và C3H7OH phản ứng là a và b (mol)
+ Ta có: a+b = 2nete = 0,16 (3)
+ m ancol phản ứng = mete + mH2O = 6,76 + 0,08.18 = 8,2 gam → 46a + 60b = 8,2 (4)
(3)(4) → a = 0,1; b = 0,06
→ Hiệu suất ete hóa của C2H5OH và C3H7OH lần lượt là: 50% và 20%
Hòa tan hoàn toàn hỗn hợp X gồm CuSO4 và KCl vào H2O, thu được dung dịch Y. Điện phân Y (có màng ngăn, điện cực trơ) đến khi H2O bắt đầu bị điện phân ở cả hai điện cực thì dừng điện phân. Số mol khí thoát ra ở anot bằng 4 lần số mol khí thoát ra ở catot. Phần trăm khối lượng của CuSO4 trong hỗn hợp X là
Đáp án B
Cu2+:x
Cl-: y
Ở catot thoát ra khí => H2O bị đp
Catot:
Cu2+ +2e → Cu
x 2x
H2O +1e → 0,5H2 + OH-
y-2x 0,5y-x
Anot:
Cl- - 1e → 0,5Cl2
y y 0,5y
=> 0,5y = 4(y-2x) => x/y=3/8
=>%mCuSO4 = 160.3/(160.3+74,5.8) = 44,61%
Cho các phát biểu sau:
(a) Các oxit của kim loại kiềm thổ phản ứng với CO tạo thành kim loại.
(b) Các kim loại Ca, Fe, Al và Na chỉ điều chế được bằng phương pháp điện phân nóng chảy.
(c) Các kim loại Mg, K và Fe đều khử được ion Ag+ trong dung dịch thành Ag.
(d) Cho Mg vào dung dịch FeCl3 dư, không thu được Fe.
Số phát biểu đúng là
Đáp án A
(a) S. Không phản ứng
(b) S. Fe được điều chế bằng phương pháp thủy luyện
(c) S. K không khử được
(d) Đ
Cho các phát biểu sau:
(a) Polietilen được điều chế bằng phản ứng trùng ngưng.
(b) Ở điều kiện thường, anilin là chất rắn.
(c) Tinh bột thuộc loại polisaccarit.
(d) Thủy phân hoàn toàn abumin của lòng trắng trứng, thu được α – aminoaxit.
(e) Ở điều kiện thích hợp, triolein tham gia phản ứng cộng hiđro.
Số phát biểu đúng là:
Đáp án B
(a) S. Điều chế bằng phản ứng trùng hợp
(b) S. Anilin ở điều kiện thường là chất lỏng
(c) Đ
(d) Đ
(e) Đ
Có 3 dung dịch riêng biệt: H2SO4 1M; KNO3 1M; HNO3 1M được đánh số ngẫu nhiên là (1), (2), (3).
- Trộn 5 ml dung dịch (1) với 5 ml dung dịch (2), thêm bột Cu dư, thu được V1 lít khí NO
- Trộn 5 ml dung dịch (1) với 5 ml dung dịch (3), thêm bột Cu dư, thu được 2V1 lít khí NO
- Trộn 5 ml dung dịch (2) với 5 ml dung dịch (3), thêm bột Cu dư, thu được V2 lít khí NO
Biết các phản ứng xảy ra hoàn toàn, NO là sản phẩm khử duy nhất, các thể tích khí đo ở cùng điều kiện. So sánh nào sau đây đúng ?
Dựa trên PT: 3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
Ta thấy dù trộn thế nào thì khi phản ứng H+ vẫn hết và NO3- dư.
→ thể tích NO thoát ra lần TN3 gấp 3 lần TN1
→ số mol axit ở TN3 gấp 3 lần ở TN1
→ TN3 trộn H2SO4 1M; HNO3 1M Và TN1 trộn KNO3 1M; HNO3 1M
→ (2) là HNO3 ; (1) là KNO3 ; (3)là H2SO4
→ TN2 có số mol H+ gấp 2 lần TN1 → V2=2V1
Cho ba hiđrocacbon mạch hở X, Y, Z (MX<MY<MZ<62) có cùng số nguyên tử cacbon trong phân tử, đều phản ứng với dung dịch AgNO3 trong NH3 dư.
Trong các phát biểu sau:
(a) 1 mol X phản ứng tối đa với 4 mol H2 (Ni, to).
(b) Chất Z có đồng phân hình học.
(c) Chất Y có tên gọi là but-1-in.
(d) Ba chất X, Y, Z đều có mạch cacbon không phân nhánh.
Số phát biểu đúng là
Đáp án D
X, Y, Z chỉ có thể là C4
X: CH≡C-C≡CH
Y: CH≡C-C=CH2
Z: CH≡C-C-CH3
(a) Đ
(b) S
(c) S
(d) Đ
Cho m gam hỗn hợp M gồm đi peptit X, tripeptit Y, tetrapeptit Z, pentapeptit T (đều mạch hở) tác dụng với dung dịch NaOH vừa đủ, thu được hỗn hợp Q gồm muối của Gly, Ala và Val. Đốt cháy hoàn toàn Q bằng một lượng oxi vừa đủ, thu lấy toàn bộ khí và hơi đem hấp thụ vào bình đựng nước vôi trong dư, thấy khối lượng bình tăng 13,23 gam và có 0,84 lít khí (đktc) thoát ra. Mặt khác, đốt cháy hoàn toàn m gam M, thu được 4,095 gam H2O. Giá trị của m gần nhất với giá trị nào sau đây?
nN2 = 0,0375 mol → nmuối = 0,075 mol → nNa2CO3 = 0,0375 mol → nNaOH = 0,075 mol
Theo PTHH : nH2O – nCO2 = ½.n muối = 0,0375 mol
Mà mbình tăng = mCO2 + mH2O = 13,23
nH2O−nCO2 = 0,0375 và
18.nH2O + 44.nCO2 = 13,23
→ nCO2=0,2025mol và nH2O = 0,24mol
→ nH = 0,48 mol
mmuối Q = mC + mH + mNa+ mO + mN
→ m muối = 12.(0,2025 + 0,0375) + 0,48 + 0,075.(23 + 14 + 16.2) = 8,535 gam
Khi đốt cháy M ta thu được : nH2O = 0,2275 mol
M + NaOH → Q + H2O
Bảo toàn nguyên tố H :
nH (trong M) + nH (trong NaOH) = nH (trong muối) + nH (trong nước)
→ nH2O = 1/2.(0,2275.2+0,075−0,24.2) = 0,025 mol
Bảo toàn khối lượng : mM + mNaOH = mQ + mH2O
→ mM = 8,535 + 0,025.18 – 0,075.40 = 5,985 gam
Đáp án cần chọn là: C

.PNG)
.PNG)
