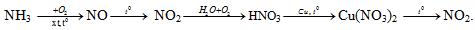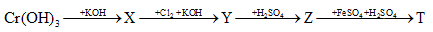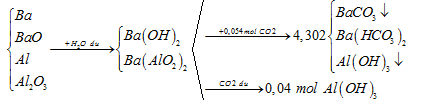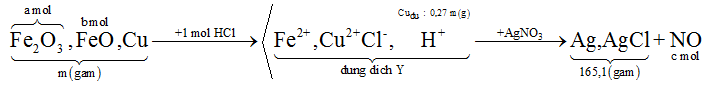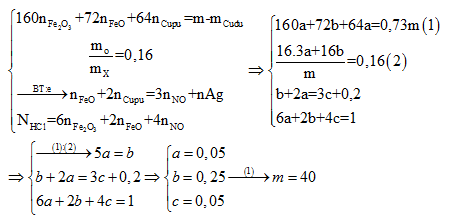Đề thi minh họa THPT QG môn Hóa học năm 2019 - Bộ GD&ĐT
Đề thi minh họa THPT QG môn Hóa học năm 2019 - Bộ GD&ĐT
-
Hocon247
-
40 câu hỏi
-
90 phút
-
58 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Kim loại nào sau đây có tính khử yếu nhất?
Sắp xếp theo dãy điện hóa: AI > Fe > Cu > Ag
Chất nào sau đây làm mất tính cứng của nuóc cứng vĩnh cửu?
Nước vĩnh cửu chứa nhiều ion Mg2+; Ca2+; Cl- và SO42-=> dùng ion CO3 2- để kết tủa hết ion Mg2+; Ca2+
Mg2+ + CO32- → MgCO3 (kết tủa)
Ca2+ + CO32 → CaCO3 (kết tủa)
Trong các chất sau, chất gây ô nhiễm không khí có nguồn gốc từ khí thải sinh hoạt là
Trong các chất sau, chất gây ô nhiễm không khí có nguồn gốc từ khí thải sinh hoạt là CO
Đáp án A
Este nào sau đây có phản ứng tráng bạc?
Este tham gia phản ứng tráng bạc => este của axit fomic
Công thức của sắt(II) hiđroxit là
Công thức của sắt(II) hiđroxit là Fe(OH)2
Polime nào sau đây có cấu trúc mạch phân nhánh?
Amilopectin có cấu trúc mạch phân nhánh
Chất nào sau đây vừa phản ứng với dung dịch HCl, vừa phản ứng vói dung dịch NaOH?
AlCl3 vừa phản ứng với dung dịch HCl, vừa phản ứng vói dung dịch NaOH
Crom có số oxi hóa +6 trong hợp chất nào sau đây?
Crom có số oxi hóa +6 trong hợp chất K2Cr2O7.
Cacbon chỉ thể hiện tính khử trong phản ứng hóa học nào sau đây?
Cacbon chỉ thể hiện tính khử trong phản ứng C + O2 → CO2
Đáp án A
Chất nào sau đây là chất hữu cơ?
Chất hữu cơ là hợp chất của c trừ CO,CO2 muối cacbonnat, muối cacbua...
Cho vài giọt nước brom vào dung dịch phenol, lắc nhẹ thấy xuất hiện
Cho vài giọt nước brom vào dung dịch phenol, lắc nhẹ thấy xuất hiện kết tủa trắng.
Cho 4,48 lít khí CO (đktc) phản ứng với 8 gam một oxit kim loại, sau khi phản ứng hoàn toàn, thu được m gam kim loại và hỗn hợp khí có tỉ khối so với Ha là 20. Giá trị của m là
nco = 0,2mol
Mhhkhí = 40g/mol
Hh khí gồm CO2 và CO dư
Áp dụng qui tắc đrrờng chéo => nco2 = 0,15mol và ncodư = 0,05mol
=> nO tách ra = nCO2 = 0,15mol
=> m = m oxit — m oxi tách ra = 8 - 0,15 . 16 = 5,6g
Cho 375 ml dung dịch NaOH 2M vào dung dịch chứa 0,2 mol AICI3, thu được m gam kết tủa.
Giá trị của m là
-Khi cho a mol OH" vào dd chứa b mol Al3+
Ta có:
\(\frac{a}{b} \le 3$\) => chỉ tạo Al(OH)t khi đó nOH- = 3nAl(OH)3
b
\(3 \le \frac{a}{b} < 4\)=> Tạo Al(OH)3 và AIO2- khi đó nAl(OH)3 = 4nAl3 + -nOH
\(\frac{a}{b} > 4\)=> Chỉ tao AlO2- => không thu đưoc kết tủa
Hướng dẫn giải
nNaOH= 0,75mol => nOH-= 0,75mol
nAl(OH)3 = 4nAl3+ - nOH-= 4.0,2 - 0,75 = 0,05mol
=> m = 3,9g
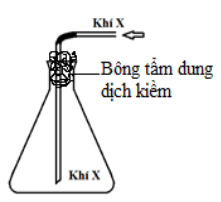
Trong phòng thí nghiệm, khí X được điều chế và thu vào bình tam giác bằng cách đẩy không khí như hình vẽ bên. Khí X là
Khí X nặng hon không khí và phản ứng vói dung dịch kiềm —> X là Clo
Phát biểu nào sau đây sai?
A sai vì Thủy phân etyl axetat: CH3COOC2H5 + H2O -> CH3COOH + C2H5OH
Đốt cháy hoàn toàn hỗn hợp metyl axetat và etyl axetat, thu được CO2 và m gam H2O. Hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 dư, thu được 25 gam kết tủa. Giá trị của m là
Phương pháp:
Đốt cháy chất có CTPT: CnH2nO2 luôn cho : nco2= nH20
Hướng dẫn giải
metyl axetat và etyl axetat có cùng CTPT dạng CnH2nO2
—>• đốt chát: nco2= nH20 = 0,25 mol —> m = 0,25.18 = 4,5
Đốt cháy hoàn toàn amin X (no, đơn chức, mạch hở) bằng O2, thu được 4,48 lít CO2 và 1,12 lít N2 (các thể tích khí đo ở đktc). Công thức phân tử của X là
Phương pháp:
+ Bảo toàn nguyên tố: namin = 2nN2
+ Chỉ sô cacbon: \(n = \frac{{{n_{C{O_2}}}}}{{{n_{a\min }}}}\)
Hướng dẫn giải
namìn = 2nN2 = 0,1
—>• Số C = nco2 / namin = 2 —> amin C2H7N
Cho sơ đồ phản ứng sau:
Mỗi mũi tên là một phản ứng hóa học. Số phản ứng mà nitơ đóng vai trò chất khử là
Phương pháp:
+ Chất khử là chất nhường electron khi tham gia phản ứng hóa học, có số oxi hóa tăng sau phản ứng
Hướng dẫn giải
nitơ là chất khử —> số oxi hóa của N tăng
\(\begin{array}{l}
\mathop N\limits^{ - 3} {H_3} \to \mathop N\limits^{ + 2} O\\
\mathop N\limits^{ + 2} O \to \mathop N\limits^{ + 4} {O_2}\\
\mathop N\limits^{ + 4} {O_2} \to H\mathop N\limits^{ + 5} {O_3}
\end{array}\)
Cho các chất sau: etyl axetat, tripanmitin, saccarozo, etylamin, Gly-Ala. số chất tham gia phản ứng thủy phân trong môi trường kiềm là
chất tham gia phản ứng thủy phân trong môi trường kiềm là etyl axetat, tripanmitin, Gly-Ala
Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl (điện cực trơ), thu được khí H2 ở catot.
(b) Cho CO dư qua hồn hợp Al2O3 và CuO đun nóng, thu được AI và Cu.
(c) Nhúng thanh Zn vào dung dịch chứa CuSO4 và H2SO4, có xuất hiện ăn mòn điện hóa.
(d) Kim loại có nhiệt độ nóng chảy thấp nhất là Hg, kim loại dẫn điện tốt nhất là Ag.
(e) Cho dung dịch AgNO3 dư vào dung dịch FeCl2, thu được chất rắn gồm Ag và AgCl.
Số phát biểu đúng là
Những phát biểu đúng là (a), (c), (d), (e).
Cho este đa chức X (có công thức phân tử C6H10O4) tác dụng vói dung dịch NaOH, thu được sản phẩm gồm một muối của axit cacboxylic Y và một ancol z. Biết X không có phản ứng tráng bạc
Số công thức cấu tạo phù hợp của X là
CTCT của X thỏa mãn là: (CH3COOCH3)2, CH3CH(COOCH3)2, (COOC2H5)2, (CH3COO)2C2H4.
Cho m gam P2O5 vào dung dịch chứa 0,1 mol NaOH và 0,05 mol KOH, thu được dung dịch X. Cô cạn X, thu được 8,56 gam hồn hợp chất rắn khan. Giá trị của m là
Giả sử kiềm có công thức chung là MOH (M=(0,1.23+0,05.39)/0,15=85/3)
Nếu phản ứng chỉ tạo 1 muối:
MH2P04 :0,15.\(\frac{{376}}{3}\) =18,8g.
M2,HPO4,\(\frac{{0,15}}{2}.\frac{{458}}{3}\) = 1 l,45g.
M3,PO4 : \(\frac{{0,15}}{2}\).180 = 9g.
mchat ran = 8,6 G < 9 g
=> MOH dư, phản ứng tạo muối M3PO4.
Đặt nM3P04= x mol, nMOH = y mol;
180x+136y/3=8,56 3x+y=nMOH=0,15
→ x=0,04, y=0,03.
→ np2O5=0,04/2=0,02 mol
→ mp205=2,84 gam.
Hỗn hợp E gồm muối vô co X (CH8N2O3) và đipeptit Y (C4H8N2O3). Cho E tác dụng với dung dịch NaOH đun nóng, thu được khí z. Cho E tác dụng với dung dịch HC1 dư, thu được khí T và chất hữu cơ. Nhận định nào sau đây sai?
E là (NH4)2CC>3; Y là H2NCH2CONHCH2COOH.
(NH4)2CO3+2NaOH → Na2CO3+2NH3(Z)+2H2O
(NH4)2CO3+2HCl → 2NH4Cl+H2O+CO2 (T)
H2NCH2CONHCH2COOH +H2O +2HCl → ClH3NCH2COOH (Q)
Hòa tan hoàn toàn Fe3O4 trong dung dịch H2SO4 (loãng, dư), thu được dung dịch X. Cho dãy gồm các chất: Cu, Fe(NO3)2, KMnO4, BaCl2, Cl2, KNO3, NaCl. số chất trong dãy phản ứng được với dung dịch X là
Dung dịch X: FeSO4, Fe2(SO4)3, H2SO4, H2O.
Những chất phản ứng vói dung dịch X là: Cu, Fe(NO3)2, KMnO4, BaCl2, Cl2, KNO3.
Chú ý: NO3- trong môi trường H+ có tính oxi hóa như HNO3
Lên men m gam tinh bột thành ancol etylic vói hiệu suất 81%, hấp thụ toàn bộ khí C02 sinh ra vào dung dịch chứa 0,05 mol Ba(OH)2, thu được kết tủa và dung dịch X. Cho từ từ dung dịch NaOH vào X, đến khi kết tủa lớn nhất thì cần ít nhất 10 ml dung dịch NaOH IM. Giá trị của m là
(C6H10O5)n + ahbO —> 2nC2H5OH + 2nCO2
noH-=2nBa(OH)2+nNaOH=0,05.2+0,01=0,l 1 mol.
=>nco2=0,5
nOH-= 0,055 mol.
=>ntinh bột=0,5nC02=0,0275 mol
=>m=0,0275.162/0,81=5,5 gam.
Cho so đồ chuyển hóa sau:
Biết X, Y, z, T là các hợp chất của crom. Chất z và T lần lượt là
Cr(OH)3+KOH → KCrO2+2H2O
2KCrO2+3Cl2+8KOH → 2K2CrO4+6KCl+4H2O
2K2CrO4+H2SO4 → K2Cr2O7+K2SO4+H2O
K2Cr2O7+6FeSO4+7H2SO4 3Fe2(SO4)3+7H2O+K2SO4+Cr2(SO4)3
3Fe2(SO4)3+7H2O+K2SO4+Cr2(SO4)3
Tiến hành thí nghiệm vói các dung dịch X, Y, z và T. Kết quả được ghi ở bảng sau:
X là Etyl fomat Y là lysin z là glucozo T là phenol
Tiến hành các thí nghiệm sau:
(a) Cho dung dịch chứa 4a mol HC1 vào dung dịch chứa a mol NaAlCl.
(b) Cho Al2O3 vào lượng dư dung dịch NaOH
(c) Sục khí CO2 đến dư vào dung dịch Ba(OH)2.
(d) Cho Fe vào dung dịch Fe2(SO4)3 dư.
(e) Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol NaHCO3.
(g) Cho Mg dư vào dung dịch HNO3 (phản ứng không thu được chất khí).
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa hai muối là
(a) A1O2- + H++ H2O → Al(OH)3
Al(OH)3 + 3H+ → Al3+ + 3H2O
2 muối: NaCl, AlCl3
a. Không tạo muối
b. Ba(HCO3)2
c. FeSO4, Fe2(SO4)3
(e) 2KHSO4+2NaHCO3 → K2SO4+Na2SO4+2H2O+2CO2
(g) Mg(NO3)2, NH4NO3
Cho 3,2 gam hồn hợp C2H2, C3H8, C2H6, C4H6 và H2 đi qua bột Ni nung nóng, sau một thời gian thu được hỗn hợp khí X. Đốt cháy hoàn toàn X cần vừa đủ V lít khí O2 (đlctc), thu được 4,48 lít CO2 (đktc). Giá trị của V là
nco2 = 4,48 : 22, 4 = 0,2 mol
BTKL mH = mhh- mc = 3,2 - 0,2.12 = 0,8 => nmo = 0,8/2 = 0,4 mol
BTNT O => no2 = (nC02 + l/2nH20 ) = 0,2 + 1/2.0,4 = 0,4 mol
V oxi (dktc) = 0,04.22,4 = 8,96 (lít)
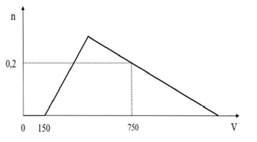
Cho từ từ dung dịch HCl IM vào dung dịch chứa X mol NaOH và y mol NaAlO2. số n mol Al(OH)3 (n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị bên. Giá trị của X và y lần lượt là
\(\begin{array}{*{20}{l}}
{{H^ + }{\mkern 1mu} {\mkern 1mu} {\mkern 1mu} + {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} O{H^ - }{\mkern 1mu} {\mkern 1mu} {\mkern 1mu} \to {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {H_2}O}\\
{0,15{\mkern 1mu} {\mkern 1mu} \leftarrow {\mkern 1mu} {\mkern 1mu} 0,15}\\
{{H^ + } + {\mkern 1mu} {\mkern 1mu} AlO_2^ - + {H_2}O \to Al{{\left( {OH} \right)}_3} \downarrow }\\
{y{\mkern 1mu} {\mkern 1mu} {\mkern 1mu} \leftarrow {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} y{\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} \to {\mkern 1mu} {\mkern 1mu} y}\\
{3{H^ + }{\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} + {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} Al{{\left( {OH} \right)}_3} \downarrow {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} \to {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} A{l^{3 + }}{\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} + {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} 3{H_2}O}\\
{3\left( {y - 0,2} \right) \leftarrow \left( {y - 0,2} \right)}
\end{array}\)
Bảo toàn H+ => \(\sum {{n_{H + }} = 0,15 + y + 3\left( {y - 0,2} \right) = 0,75} \)
=> y = 0,3 mol
nNaOH = nH+ = 0,15 (mol)
Vậy X = 0,15 mol; y = 0,3 mol
Cho các chất sau: metan, etilen, buta-1,3-dien, benzen, toluen, stiren, phenol, metyl acrylat.
Số chất tác dụng được với nước brom ở điều kiện thường là
Số chất tác dụng được vói nước brom ở điều kiện thường là : etilen, buta-l,3-đien, stiren, phenol, metyl acrylat
Điện phân (điện cực tro, màng ngăn xốp) dung dịch gồm CuSO4 và NaCl (tỉ lệ mol tưong ứng 1 : 3) với cường độ dòng điện l,34A. Sau thòi gian t giờ, thu được dung dịch Y (chứa hai chất tan) có khối lượng giảm 10,375 gam so vói dung dịch ban đầu. Cho bột AI dư vào Y, thu được 1,68 lít khí H2 (đlctc). Biết các phản ứng xảy ra hoàn toàn, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hoi của nước. Giá trị của t là
Do dung dịch sau điện phân chứa 2 chất là: Na2SO4 và NaOH. Tỉ lệ mol CuSO4 và NaCl là 1:3 nên Cu2+ bị điện phân hết truóc.
A1 + OH- → AlO2‑+ 1,5H2
=>noH-=nH2/l,5=0,05 mol.
Quá trình điện phân:
Cu2+ + 2Cl - → Cu + Cl2
a 2a a a
2Cl- + 2H2O → Cl2 + H2 + 2OH-
a(=3a-2a) 0,5a 0,5a a=0,05
m giảm 64a + 71a + 71.0,5a + 2.0,5a = 8,575 gam < 10,375
=> H2O bị điện phân: mH20= 10,375-8,575 = 1,8 gam
H2O → H2+0,5O2
0,1 0,1 0,05 mol
Tại anot: 0,075 mol Cb, 0,05 mol O2
=> ne= 0,075.2 + 0,05.4 = 0,35 mol=> t = ne.96500/I=0,35.96500/1,34=25205,2 giây = 7 giờ.
Đốt cháy hoàn toàn a gam este hai chức, mạch hở X (được tạo bởi axit cacboxylic no và hai ancol) cần vừa đủ 6,72 lít khí O2 (đktc), thu được 0,5 mol hỗn hợp CO2 và H2O. Cho a gam X phản ứng hoàn toàn với 200 ml dung dịch NaOH IM, thu được dung dịch Y. Cô cạn Y, thu được m gam chất rắn khan.
Giá trị của m là
X có dạng CnH2n-2kO4
nCO2 = x; nH2O = y → x + y = 0,5 (1)
Bảo toàn O: 2nCO2 + nH2O = 2.0,3 + 4nx (2)
Ta có nCO2 - 11H2O = k.nx (3)
(1), (2), (3) —>1 nCO2 = 0,3; nmo = 0,2; nx=0,05; k=l
—> Y tạo bởi axit 2 chức no, mạch hở và 1 ancol no, mạch hở và 1 ancol ko no (1 lk TÌ), mạch hở CTCT Y:
COO -CH3
COO – CH2 -CH = CH2
mchấtrắn = mNaOHdư + m(COONa)2 = 0,1.40 + 0,05.134 = 10,7 gam
Hòa tan hoàn toàn m gam hỗn hợp X gồm Ba, BaO, Al và AI2O3 vào nước (dư), thu được 0,896 lít khí (đktc) và dung dịch Y. Hấp thụ hoàn toàn 1,2096 lít khí CO2 (đlctc) vào Y, thu được 4,302 gam kết tủa. Lọc kết tủa, thu được dung dịch z chỉ chứa một chất tan. Mặt khác, dẫn từ từ CO2 đến dư vào Y thì thu được 3,12 gam kết tủa. Giá trị của m là
\(\begin{array}{l}
BTKL \Rightarrow {n_{BaC{O_3}}} = \frac{{4,302 - {m_{Al{{\left( {OH} \right)}_3}}}}}{{197}} = \frac{{4,032 - 3,12}}{{197}} = 0,006mol\\
BTNTC \Rightarrow {n_{Ba{{\left( {HC{O_3}} \right)}_2}}} = \frac{{{n_{C{O_2}}} - {n_{BaC{O_3}}}}}{2} = \frac{{0,054 - 0,006}}{2} = 0,024mol\\
BTNT\,\,Ba\,:{n_{Ba}} = {n_{BaC{O_3}}} + {n_{Ba{{\left( {HC{O_3}} \right)}_2}}} = 0,006 + 0,024 = 0,03mol
\end{array}\)
nAl = nAl(OH)3 = 0,04 mol
\({\rm{X}}\left\{ \begin{array}{l}
{\rm{Ba:0,03}}\,{\rm{mol}}\\
{\rm{Al:}}\,{\rm{0,04}}\,{\rm{mol}}\\
{\rm{O:a}}\,\,{\rm{mol}}
\end{array} \right.\)
BT electron :2nBa + 3nAl = 2nO + 2nH2
=> 2.0,03 + 3. 0,04 = 2a + 2.0,04=> a = 0.05 mol
=> m = 0,03.137 + 0,04.27 + 0,05.16 = 5,99g
Hỗn hợp X chứa hai amin kế tiếp thuộc dãy đồng đẳng của metylamin. Hỗn hợp Y chứa glyxin và lysin. Đốt cháy hoàn toàn 0,2 mol hồn hợp z (gồm X và Y) cần vừa đủ 1,035 mol O2, thu được 16,38 gam H2O; 18,144 lít (đktc) hỗn hợp CO2 và N2. Phần trăm khối lượng của amin có khối lượng phân tử nhỏ hon trong z là
Z bao gồm:
CnH2n+3N: a mol
C2H5NO2: b mol
C6H14N2O2 : c mol
=> nCO2 = na + 2b + 6c và nN2 = a/2 + b/2 + c
= > nCO2 + nN2 = na + a/2 + 5b/2 + 7c = 0,81 (1 )
nH20= a(2n + 3)/2 + 5b/2 + 7c = 0,91 (2)
(1) => a = 0,1
nz = 0,2 => b + c = 0,1 (3)
Bảo toàn O:
2(b + c) + 2no2 - 2nco2 + 11H20 —> nco2 = 0,68 => nN2 = a/2 + b/2 + c = 0,81 - 0,68 (4)
(4) =>b = 0,04 và c = 0,06
nco2 = na + 2b + 6c = 0,68 => n = 2,4
=> X chứa C2H7N (0,06) và C3H9N (0,04) (Tính dựa vào c trung bình 2,4 và tổng số mol a = 0,1 )
Vậy z chứa C2H7N (0,06); C3H9N (0,04); C2H5NO2 (0,04) và C6H14N2O2 (0,06)
=> %C2H7N = 16,05%
Hỗn hợp X gồm Fe2O3, FeO và Cu (trong đó nguyên tố oxi chiếm 16% theo khối lượng). Cho m gam X tác dụng với 500 ml dung dịch HCl 2M (dư), thu được dung dịch Y và còn lại 0,27m gam chất rắn không tan. Cho dung dịch AgNO.3 dư vào Y, thu được khí NO (sản phẩm khử duy nhất của N+5) và 165,1 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Xét hỗn hợp kết tủa ta có: nAgCl = nHCl = 1 mol
→ nAgCl = \(\frac{{{\rm{m - 143,5nAgCl}}}}{{{\rm{108}}}}{\rm{ = }}\frac{{{\rm{165,1 - 143,4}}{\rm{.1}}}}{{{\rm{108}}}}{\rm{ = 0,2}}\,\,{\rm{mol}}\)
Khi cho X tác dụng với HCl và dung dịch Y tác dụng vói AgNO3 thì ta có hệ sau:
Cho hỗn hợp z gồm peptit mạch hở X và amino axit Y (Mx> 4My) vói tỉ lệ mol tưong ứng 1:1. Cho m gam z tác dụng vừa đủ vói dung dịch NaOH, thu được dung dịch T chứa (m + 12,24) gam hỗn hợp muối natri của glyxin và alanin. Dung dịch T phản ứng tối đa với 360 ml dung dịch HCl 2M, thu được dung dịch chứa 63,72 gam hỗn hợp muối. Các phản ứng xảy ra hoàn toàn. Kết luận nào sau đây đúng?
Dung dịch G chứa GlyNa (a mol) và ValNa (b mol)
=> nHCl = 2a + 2b = 0,72
và 1 ll,5a + 125,5b + 58,5(a + b) = 63,72
=> a = b = 0,18
=> nNaOH = a + b = 0,36 lTLNaOH - mH20 = 12,24 => nmo = 0,12 => nx= ny = 0,06
X có k gốc amino axit => 0,06k + 0,06 = 0,36 => k = 5
TH1 : X là Gly3Ala2 và Y là Ala (Loại Vì Mx < 4My)
TH2: X là Gly2Ala3 và Y là Gly (Thỏa mãn Mx > 4My)
A. Sai, Y có %N = 18,67%
B. Sai, X có 4 liên kết peptit.
C. Sai
D. Đúng.
Hòa tan hoàn toàn 15,6 gam hỗn hợp gồm Fe, Fe3O4, Fe2O3, Mg, MgO và CuO vào 200 gam dung dịch H2SO4 và NaNO3, thu được dung dịch X chỉ chứa muối sunfat trung hòa của kim loại, hồn hợp khí Y gồm 0,01 mol N2O và 0,02 mol NO. Cho X phản ứng với dung dịch Ba(OH)2 dư, thu được 89,15 gam kết tủa. Lọc kết tủa nung trong không khí đến khối lượng không đổi, thu được 84,386 gam chất rắn. Nồng độ phần trăm của FeS04 trong X có giá trị gần nhất với giá trị nào sau đây?
Bảo toàn N => nNaN03 = 2n\20 + n\o = 0,04
Đặt nH2S04 = a và no trong hỗn hợp ban đầu = b
=> nH+ = 2a = 2b +0,01.10+ 0,02.4(1 )
nBa(OH)2 = nBaS04 = a
nNaOH= nNaN03 = 0,04
Bảo toàn OH- => nOHtrong = 2a - 0,04
=> m kết tủa = 233a + (15,6 - 16b) + 17(2a - 0,04) = 89,15 (2)
(1)(2) => a = 0,29 và b = 0,2
Đặt nFe2+ = c
Bảo toàn electron => nO2 phan ưng với kết tủa = 0,25c
Bảo toàn H => nH2O khi nung kết tủa = a - 0,02 = 0,27
m rắn = 89,15 + 32.0,25c - 18.0,27 = 84,386
=>c = 0,012
mddx= 15,6 + 200 - m Y = 214,56
=> C%FeS04 = \(\frac{{0,012.152}}{{214,56}}\) .100% = 0,85%
Cho các chất hữu co mạch hở: X là axit không no có hai liên kết 71 trong phân tử, Y là axit no đơn chức, z là ancol no hai chức, T là este của X, Y với z. Đốt cháy hoàn toàn a gam hỗn hợp M gồm X và T, thu được 0,1 mol CO2 và 0,07 mol H2O. Cho 6,9 gam M phản ứng vừa đủ với dung dịch NaOH, cô cạn dung dịch sau phản ứng thu được hỗn hợp muối khan E. Đốt cháy hoàn toàn E, thu được Na2CO3; 0,195 mol CO2 và 0,135 mol H2O. Phần trăm khối lượng của T trong M có giá trị gần nhất với giá trị nào sau đây?
Gọi CTTQ của X và T là CnH2n-2O2 (n>3) và CmH2m-4O4 (m>6)
+ Bảo toàn nguyên tố C, H
+ Bảo toàn khối lượng