Chia hỗn hợp X gồm Fe và FeO thành hai phần bằng nhau. Phần 1 phản ứng vừa đủ với 0,1 mol HCl. Phần 2 đem hòa tan hết trong 15 gam dung dịch H2SO4 98% đun nóng thu được dung dịch Y và 1,232 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Nồng độ phần trăm của H2SO4 trong dung dịch Y là
A. 13,07 %.
B. 13,42%.
C. 10,82%.
D. 12,47%.
Lời giải của giáo viên
 ToanVN.com
ToanVN.com
Đáp án B
Quan sát nhanh: \(\left\{ {\begin{array}{*{20}{l}} {{\text{Fe}}} \\ {{\text{FeO}}} \end{array}} \right\}{\mkern 1mu} {\mkern 1mu} {\text{ + }}{\mkern 1mu} {\mkern 1mu} \underbrace {{\text{HCl}}}_{0,1{\text{mol}}} \to {\text{FeC}}{{\text{l}}_{\text{2}}}{\mkern 1mu} {\mkern 1mu} {\text{ + }}{\mkern 1mu} {\mkern 1mu} \left\{ {\begin{array}{*{20}{l}} {{{\text{H}}_{\text{2}}}} \\ {{{\text{H}}_{\text{2}}}{\text{O}}} \end{array}} \right\}.\)
⇒ nFeCl2 = 0,05 mol. Quy đổi X gồm 0,05 mol Fe và ? mol O.
☆ Phần 2: \(\left\{ {\begin{array}{*{20}{l}} {{\text{Fe}}} \\ {\text{O}} \end{array}} \right\}{\mkern 1mu} {\mkern 1mu} {\text{ + }}{\mkern 1mu} {\mkern 1mu} {{\text{H}}_{\text{2}}}{\text{S}}{{\text{O}}_{\text{4}}} \to \underbrace {{\text{F}}{{\text{e}}_2}{{({\text{S}}{{\text{O}}_4})}_3}}_{0,025{\text{mol}}}{\mkern 1mu} {\mkern 1mu} {\text{ + }}{\mkern 1mu} \underbrace {{\mkern 1mu} {\text{S}}{{\text{O}}_2}}_{0,055{\text{mol}}}{\mkern 1mu} {\mkern 1mu} {\text{ + }}{\mkern 1mu} {\mkern 1mu} {{\text{H}}_2}{\text{O}}.\)
Bảo toàn nguyên tố Fe ⇒ có 0,025 mol Fe2(SO4)3
|→ tiếp tục bảo toàn nguyên tố S ta có nH2SO4 phản ứng = 0,13 mol.
⇒ lượng axit H2SO4 còn dư trong dung dịch Y là 0,02 mol.
☆ Yêu cầu tính C% H2SO4 dư trong Y nên cần tính khối lượng dung dịch Y.
Theo bảo toàn electron ta có: 3nFe = 2nO trong oxit + 2nSO2 ⇒ nO trong X = 0,02 mol.
⇒ mX = 3,12 gam ⇒ mdung dịch Y = 15 + 3,12 – 0,055 × 64 = 14,6 gam.
Vậy, C%H2SO4 trong Y = 0,02 × 98 ÷ 14,6 × 100% ≈ 13,42%.
CÂU HỎI CÙNG CHỦ ĐỀ
Cho 200 gam dung dịch KOH 5,6% vào dung dịch CuCl2 dư. Sau khi phản ứng xảy ra hoàn toàn, kết tủa thu được có khối lượng là
Để trung hòa 25 gam dung dịch của một amin đơn chức X nồng độ 12,4% cần dùng 100 ml dung dịch HCl 1M. Công thức phân tử của X là
Ở điều kiện thường, chất nào sau đây không phản ứng với dung dịch H2SO4 loãng?
Phân đạm cung cấp nitơ hóa hợp cho cây trồng, có tác dụng kích thích quá trình sinh trưởng, giúp cây phát triển nhanh, cho nhiều hạt, củ, quả. Chất nào sau đây không phải là phân đạm?
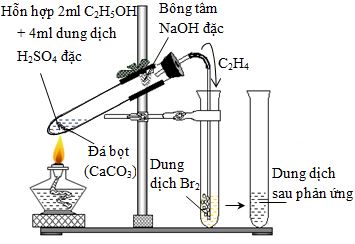
Cho hình vẽ bên mô tả thí nghiệm điều chế và thử tính chất của etilen. Phát biểu nào sau đây sai khi nói về thí nghiệm đó?
Nước mía chiếm 70% khối lượng của cây mía. Lượng saccarozơ trong nước mía ép là khoảng 20%. Khối lượng saccarozơ thu được từ 1,0 tấn mía nguyên liệu (cho biết hiệu suất của toàn bộ quá trình là 80%) là
Cho sơ đồ các phản ứng sau:
(a) C4H6O2 (X) + NaOH → (Y) + (Z).
(b) (Z) + AgNO3 + NH3 +H2O → (F) + Ag↓ + NH4NO3.
(c) (F) + NaOH → (Y) + NH3↑ + H2O.
Chất X là
Tiến hành các thí nghiệm sau:
(1) Cho dung dịch NaOH vào dung dịch Ba(HCO3)2.
(2) Cho dung dịch NH3 đến dư vào dung dịch AlCl3.
(3) Sục khí CO2 tới dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4]).
(4) Cho dung dịch AgNO3 vào dung dịch MgCl2.
(5) Sục khí H2S vào dung dịch FeCl2.
(6) Cho Mg vào dung dịch FeCl3 dư.
Sau khi các phản ứng kết thúc, có bao nhiêu thí nghiệm thu được kết tủa?
Trong phòng thí nghiệm, khí H2 được điều chế bằng phản ứng giữa Zn và dung dịch H2SO4 loãng. Khí H2 sẽ thoát ra nhanh hơn khi thêm vào hệ phản ứng vài giọt dung dịch nào sau đây?
Sản phẩm của phản ứng este hóa giữa ancol metylic và axit propionic là
Kim loại nào sau đây không điều chế được bằng phương pháp thủy luyện?
Thủy phân hoàn toàn 1 mol saccarozơ trong môi trường axit thu được